خلات النيكل، مع الصيغة Ni(CH3COO)2، مركب كيميائي. يتم استخدامه في العديد من الصناعات، بما في ذلك الطلاء الكهربائي وتركيب المحفزات، وذلك بسبب مكوناته من النيكل والأسيتات.
| اسم الأيوباك | خلات النيكل |
| الصيغة الجزيئية | ني (CH3COO)2 |
| CAS رقم | 373-02-4 |
| المرادفات | ملح النيكل من حمض الخليك، ثنائي أسيتات النيكل، خلات النيكل |
| إنتشي | InChI=1S/2C2H4O2.Ni/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
خصائص خلات النيكل
صيغة خلات النيكل
الصيغة الكيميائية لثنائي أسيتات النيكل هي Ni(CH3COO)2. وهذا يعني أن كل جزيء ثنائي أسيتات النيكل يحتوي على ذرة Ni واحدة مرتبطة بأيونات CH3COO.
خلات النيكل الكتلة المولية
تبلغ الكتلة المولية لثنائي أسيتات النيكل حوالي 176.7 جم / مول. يتم حساب هذه القيمة عن طريق جمع الكتل الذرية لذرة نيكل واحدة وأربع ذرات أكسجين من أيونات الأسيتات.
نقطة غليان خلات النيكل
يحتوي ثنائي أسيتات النيكل على نقطة غليان تبلغ حوالي 140 درجة مئوية (284 درجة فهرنهايت). وعند هذه الدرجة يتغير المركب من حالته السائلة إلى الحالة الغازية.
نقطة انصهار خلات النيكل
تبلغ نقطة انصهار ثنائي أسيتات النيكل حوالي 140 درجة مئوية (284 درجة فهرنهايت). هذه هي درجة الحرارة التي يتحول عندها المركب الصلب إلى سائل.
كثافة خلات النيكل جم/مل
تبلغ كثافة ثنائي أسيتات النيكل حوالي 1.744 جم / مل. تمثل قيمة الكثافة كتلة المركب لكل وحدة حجم وتستخدم عادة لوصف السوائل.
خلات النيكل الوزن الجزيئي
الوزن الجزيئي لثنائي أسيتات النيكل، ويسمى أيضًا الوزن الجزيئي، هو 176.7 جم/مول. يتم حساب هذه القيمة عن طريق إضافة الأوزان الذرية لجميع الذرات الموجودة في المركب.
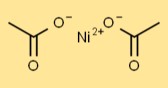
هيكل خلات النيكل
يتضمن هيكل ثنائي أسيتات النيكل ذرة Ni مركزية مرتبطة بأيونات CH3COO. تساهم أيونات الأسيتات في التنسيق حول ذرة النيكل، مما يمنحها هندسة محددة.
ذوبان خلات النيكل
ثنائي أسيتات النيكل ذو ذوبان معتدل في الماء. يمكن أن تذوب في الماء لتكوين محلول. يمكن أن تختلف القابلية للذوبان اعتمادًا على درجة الحرارة ووجود مواد أخرى في المحلول.
| مظهر | مسحوق بلوري أخضر |
| جاذبية معينة | ~1,744 جم/مل |
| لون | أخضر |
| يشم | عديم الرائحة |
| الكتلة المولية | ~176.7 جرام/مول |
| كثافة | ~1,744 جم/مل |
| نقطة الانصهار | ~140 درجة مئوية (284 درجة فهرنهايت) |
| نقطة الغليان | ~140 درجة مئوية (284 درجة فهرنهايت) |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | معتدل |
| الذوبان | قابل للذوبان في المذيبات المختلفة |
| ضغط البخار | غير موثقة بشكل جيد |
| كثافة بخار | غير موثقة بشكل جيد |
| pKa | غير موثقة بشكل جيد |
| الرقم الهيدروجيني | غير موثقة بشكل جيد |
سلامة ومخاطر خلات النيكل
يشكل ثنائي أسيتات النيكل مخاطر محتملة على السلامة. قد يهيج الجلد والعينين والجهاز التنفسي عن طريق الاتصال أو الاستنشاق. تجنب ابتلاعه لأن ذلك قد يسبب آثارًا ضارة. والتهوية الكافية ضرورية لتجنب استنشاق أبخرتها. عند التعامل، قم بارتداء معدات الحماية المناسبة مثل القفازات والنظارات الواقية. التخلص منها بشكل صحيح وتجنب إطلاقها في البيئة. إذا تعرضت، اطلب الرعاية الطبية. اتبع أوراق بيانات السلامة والتوجيهات عند استخدام ثنائي أسيتات النيكل لتقليل المخاطر المرتبطة بالتعامل معها وتخزينها والتخلص منها.
| رموز الخطر | المخاطر الصحية |
| وصف الأمان | يسبب تهيج الجلد والعين. ضار إذا ابتلع أو استنشق. تجنب إطلاقها في البيئة. ارتداء معدات الحماية. اطلب الرعاية الطبية إذا تعرضت لها. |
| أرقام تعريف الأمم المتحدة | UN3077 (الفئة 9) |
| رمز النظام المنسق | 2915.12.00 |
| فئة الخطر | 9 (البضائع الخطرة المتنوعة) |
| مجموعة التعبئة | ثالثا |
| تسمم | سمية معتدلة. قد يسبب تهيجًا وتلفًا في حالة ابتلاعه أو استنشاقه أو ملامسته للجلد أو العينين. |
طرق تصنيع خلات النيكل
يمكن تصنيع ثنائي أسيتات النيكل بطرق مختلفة. الطريقة الشائعة هي تفاعل أكسيد النيكل (NiO) أو كربونات النيكل (NiCO3) مع حمض الأسيتيك (CH3COOH) أو مشتقاته. يحدث هذا التفاعل تحت ظروف خاضعة للرقابة، مما يؤدي إلى تكوين ثنائي أسيتات النيكل والماء كمنتجات ثانوية. تتضمن الطريقة الأخرى معالجة النيكل المعدني أو هيدروكسيد النيكل (Ni(OH)2) بحمض الأسيتيك أو أملاحه، مما يسهل تكوين ثنائي أسيتات النيكل.
بالإضافة إلى ذلك، يمكن استخدام عملية الترسيب عن طريق خلط ملح النيكل القابل للذوبان، مثل كلوريد النيكل (NiCl2)، مع ملح خلات قابل للذوبان. يؤدي هذا الخليط إلى ترسيب ثنائي أسيتات النيكل من المحلول، والذي يمكن بعد ذلك فصله وتجميعه. يساعد تعديل درجة الحموضة بعناية خلال هذه العملية على تحقيق أفضل النتائج.
تعتبر طرق التوليف هذه ضرورية لإنتاج ثنائي أسيتات النيكل لمختلف التطبيقات، بما في ذلك استخدامه كمحفز ومقدم في التفاعلات الكيميائية. يعتمد اختيار الطريقة على عوامل مثل النقاء المطلوب والكفاءة وحجم الإنتاج.
استخدامات خلات النيكل
يجد ثنائي أسيتات النيكل تطبيقات متعددة الاستخدامات في العديد من الصناعات نظرًا لخصائصه المميزة وتركيبه الكيميائي. بعض الاستخدامات الهامة تشمل:
- الطلاء الكهربائي: يعمل ثنائي أسيتات النيكل كمصدر لأيونات النيكل في عمليات الطلاء الكهربائي. إنه يسهل ترسيب طبقة رقيقة من النيكل على ركائز مختلفة، مما يحسن مقاومة التآكل ويوفر لمسة نهائية زخرفية.
- تخليق المحفز: يستخدمه الكيميائيون كمقدمة لإنشاء محفزات لتفاعلات كيميائية متعددة. تعتمد الصناعات مثل البتروكيماويات والأدوية بشكل كبير على المحفزات المحتوية على النيكل.
- صناعة النسيج: في عمليات صباغة النسيج، يساعد على تثبيت الأصباغ على ألياف النسيج، وتحسين التصاق الصبغة وثبات اللون.
- الكاشف المختبري: يستخدم العلماء ثنائي أسيتات النيكل ككاشف لاكتشاف وتحديد مركبات معينة، مما يسمح لهم باختبار مجموعات وظيفية محددة.
- المعالجة السطحية: يستخدمه المصنعون في تطبيقات المعالجة السطحية، مثل إنتاج لوحات الدوائر المطبوعة. يساعد على تكوين طبقة واقية على الأسطح النحاسية.
- التخليق العضوي: في تفاعلات التخليق العضوي المختلفة، تلعب ثنائي أسيتات النيكل دورًا حاسمًا في تكوين روابط الكربون والكربون والكربون والذرة غير المتجانسة.
- تنقية الغاز: يلعب دوراً رئيسياً في عمليات تنقية الغاز، وخاصةً في إزالة الشوائب مثل كبريتيد الهيدروجين من الغازات الصناعية.
- الكيمياء التحليلية: ثنائي أسيتات النيكل هو كاشف قياسي في الكيمياء التحليلية، يستخدم لأغراض المعايرة ومراقبة الجودة.
بشكل عام، تسلط التطبيقات المتنوعة لثنائي أسيتات النيكل الضوء على أهميته عبر الصناعات، بدءًا من تحسين جماليات المنتج وحتى المساعدة في التحولات والعمليات الكيميائية الهامة.
أسئلة:
س: هل يمكن خلط الأسيتال والنيكل في حلقة واحدة؟
ج: لا يُنصح عمومًا بخلط الأسيتال والنيكل في الإبزيم، حيث يمكن أن يتفاعل الأسيتال مع معادن معينة، مما قد يسبب تآكلًا وتلفًا لمكونات الإبزيم.
س: ما هي الصيغة الصحيحة لمركب خلات النيكل الأيوني؟
ج: الصيغة الصحيحة لثنائي أسيتات النيكل، وهو مركب أيوني، هي Ni(CH3COO)2.
س: هل لخلات النيكل (2) + بروميد الحديد (2) صيغة تجريبية؟
ج: ثنائي أسيتات النيكل (II) وبروميد الحديد (II) لا يشكلان مركبًا مباشرًا، لذلك لا يمكن تطبيق الصيغة التجريبية.
س: ما هي كتلة الماء من الأسيتال والنيكل؟
ج: تشير كتلة الماء المصنوعة من الأسيتال والنيكل إلى مكون التبريد المستخدم في أنظمة التبريد السائل للكمبيوتر الشخصي، وعادةً ما تكون مصنوعة من بلاستيك الأسيتال وتتميز بسطح مطلي بالنيكل.
س: ما هي معدلات تفاعل النيكل والنحاس مع حمض الأسيتيك؟
ج: يتفاعل النيكل والنحاس ببطء مع حمض الأسيتيك، ويطلقان غاز الهيدروجين ويشكلان أملاح ثنائي الأسيتات الخاصة بهما.
س: كيف يمكن صنع خلات النيكل؟
ج: يمكن تصنيع ثنائي أسيتات النيكل عن طريق تفاعل أكسيد النيكل أو كربونات النيكل مع حمض الأسيتيك، ثم التبلور والتنقية.
س: كيفية إزالة خلات النيكل؟
ج: تخلص من ثنائي أسيتات النيكل كنفايات خطرة وفقًا للوائح المحلية. ومن المهم استشارة سلطات إدارة النفايات لمعرفة طرق التخلص المناسبة.
س: ما هي صيغة خلات النيكل (2)؟
ج: صيغة ثنائي أسيتات النيكل (II) هي Ni(CH3COO)2.
س: هل خلات النيكل قابلة للذوبان؟
ج: نعم، ثنائي أسيتات النيكل قابل للذوبان بشكل معتدل في الماء، ويشكل محلولاً يمكن استخدامه في مجموعة متنوعة من التطبيقات.
