ثنائي ميثيل أمين (DMA) هو مركب كيميائي ذو رائحة مريبة. يتم استخدامه في العمليات الصناعية المختلفة، مثل إنتاج المواد الكيميائية الزراعية والأدوية والمواد الخافضة للتوتر السطحي.
| اسم الأيوباك | ن- ميثيل ميثانامين |
| الصيغة الجزيئية | C2H7N |
| CAS رقم | 124-40-3 |
| المرادفات | DMA، ن- ميثيل ميثانامين، ثنائي ميثيل أمونيا، ميثيل أمين، ن- ميثيل ميثانامين، ن- ميثيل ميثانامين، ن- ميثيل ميثانامين هيدروكلوريد |
| إنتشي | إنتشي = 1S/C2H7N/c1-3-2/h3H،1-2H3 |
خصائص ثنائي ميثيل أمين
صيغة ثنائي ميثيل أمين
ثنائي ميثيل أمين هو مركب عضوي له الصيغة الكيميائية C2H7N. وهو أحد مشتقات الأمونيا، حيث تم استبدال اثنتين من ذرات الهيدروجين الثلاث بمجموعات الميثيل. وتمثل صيغته تركيب جزيء ثنائي ميثيل أمين، الذي يحتوي على ذرتي كربون وسبع ذرات هيدروجين وذرة نيتروجين واحدة.
ثنائي ميثيل أمين الكتلة المولية
الكتلة المولية لـ DMA هي 45.09 جم/مول. وهو جزيء صغير نسبيًا، مما يساهم في انخفاض نقطة غليانه وارتفاع ضغط البخار. الكتلة المولية هي كتلة مول واحد من DMA ويتم حسابها عن طريق إضافة الكتل الذرية لجميع الذرات الموجودة في الجزيء.
نقطة غليان ثنائي ميثيل أمين
نقطة غليان DMA هي -6.3 درجة مئوية. نقطة الغليان المنخفضة هذه تجعل من DMA سائلًا متطايرًا وقابلاً للاشتعال. ويغلي عند درجة حرارة أقل من الماء، مما يعني أنه يمكن أن يتبخر بسهولة عند تعرضه للهواء. نقطة غليان المادة هي درجة الحرارة التي تتحول عندها من الحالة السائلة إلى الحالة الغازية.
نقطة انصهار ثنائي ميثيل أمين
نقطة انصهار DMA هي -92 درجة مئوية. وهو سائل عديم اللون في درجة حرارة الغرفة ولكن يمكن أن يتجمد ليشكل مادة صلبة بلورية بيضاء تحت نقطة الانصهار. نقطة انصهار المادة هي درجة الحرارة التي تتحول عندها من الحالة الصلبة إلى الحالة السائلة.
كثافة ثنائي ميثيل أمين جم / مل
كثافة DMA هي 0.67 جم/مل. وهو أقل كثافة من الماء الذي تبلغ كثافته 1 جم / مل. وهذا يعني أن DMA سوف يطفو على الماء. كثافة المادة هي الكتلة لكل وحدة حجم المادة.
الوزن الجزيئي لثنائي ميثيل أمين
الوزن الجزيئي لـ DMA هو 45.09 جم/مول. إنه مجموع الأوزان الذرية لجميع الذرات الموجودة في جزيء DMA. الوزن الجزيئي مفيد في تحديد كمية المادة اللازمة لإنتاج حجم معين أو تركيز معين من المحلول.
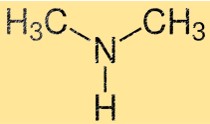
هيكل ثنائي ميثيل أمين
يتكون هيكل DMA من ذرة نيتروجين مرتبطة بمجموعتي ميثيل وذرة هيدروجين. وهو أمين أساسي بسيط ذو شكل هرمي. تحتوي ذرة النيتروجين على زوج من الإلكترونات الوحيدة، مما يجعل DMA قاعدة ضعيفة.
ذوبان ثنائي ميثيل أمين
DMA قابل للذوبان في الماء والإيثانول وثنائي إيثيل الأثير. فهو يشكل روابط هيدروجينية مع جزيئات الماء، مما يسمح له بالذوبان بسهولة في الماء. ترجع قابليته للذوبان في المذيبات العضوية مثل الإيثانول وثنائي إيثيل الأثير إلى قدرته على تكوين روابط هيدروجينية بين الجزيئات مع جزيئات المذيب.
| مظهر | سائل عديم اللون |
| جاذبية معينة | 0.666 جم/مل عند 25 درجة مئوية |
| لون | عديم اللون |
| يشم | الأسماك والأمونيا |
| الكتلة المولية | 45.09 جرام/مول |
| كثافة | 0.666 جم/مل عند 25 درجة مئوية |
| نقطة الانصهار | -92 درجة مئوية |
| نقطة الغليان | -6.3 درجة مئوية |
| نقطة فلاش | -32 درجة مئوية |
| الذوبان في الماء | يذوب في الماء |
| الذوبان | قابل للذوبان في الإيثانول وثنائي إيثيل الأثير |
| ضغط البخار | 522 ملم زئبق عند 20 درجة مئوية |
| كثافة بخار | 1.53 (الهواء = 1) |
| pKa | 10.73 |
| الرقم الهيدروجيني | 11.1 |
سلامة ومخاطر ثنائي ميثيل أمين
يمكن أن يكون DMA خطيرًا إذا لم يتم التعامل معه بشكل صحيح. وهو شديد الاشتعال ويمكن أن يشتعل بسهولة في وجود الحرارة أو الشرر أو اللهب. كما أنه سام ويمكن أن يسبب تهيجًا للعينين والجلد والجهاز التنفسي. التعرض المباشر لـ DMA يمكن أن يسبب الصداع والدوخة والغثيان. ومن المهم استخدام معدات الحماية مثل القفازات والنظارات الواقية وأجهزة التنفس عند التعامل مع DMA. يجب أن يتم تخزينه في مكان بارد وجاف، بعيدا عن الحرارة ومصادر الاشتعال. في حالة الانسكاب أو التعرض، يجب التعامل معه وفقًا لبروتوكولات السلامة المناسبة.
| رموز الخطر | ف، ت |
| وصف الأمان | شديدة الاشتعال والسامة والتآكل |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 1032 |
| رمز النظام المنسق | 2921.19.00 |
| فئة الخطر | 2.1 (غاز قابل للاشتعال) |
| مجموعة التعبئة | ثانيا |
| تسمم | الجرعة المميتة 50 (عن طريق الفم، للفئران) 230 ملغم/كغم؛ التركيز المميت للنصف (استنشاق، الفئران) 1660 جزء في المليون/4 ساعات |
طرق تخليق ثنائي ميثيل أمين
توجد عدة طرق لتجميع DMA.
تتضمن الطريقة الشائعة تفاعل الميثانول والأمونيا في وجود محفز. يمكن للكيميائيين تقطير وتنقية المنتج الناتج للحصول على DMA نقي.
تتضمن الطريقة الأخرى تفاعل الفورمالديهايد وكلوريد الأمونيوم في وجود قاعدة، مثل هيدروكسيد الصوديوم. ينتج عن التفاعل ميثيل أمين، والذي يمكن بعد ذلك تفاعله مع الفورمالديهايد ليعطي DMA.
لتصنيع DMA، يمكن التفاعل مع ثنائي ميثيل سلفات والأمونيا . هذا التفاعل طارد للحرارة وينتج DMA وكبريتات الأمونيوم كمنتجات ثانوية. ومع ذلك، لا يستخدم الكيميائيون هذه الطريقة عادة بسبب الطبيعة الخطرة لكبريتات ثنائي الميثيل.
للحصول على DMA، يمكن تفاعل كلوريد الميثيل مع الأمونيا . ينتج عن هذا التفاعل أيضًا كلوريد الأمونيوم كمنتج ثانوي.
بشكل عام، يتطلب تركيب DMA معالجة دقيقة واستخدام المعدات المناسبة ومعدات الحماية بسبب الطبيعة الخطرة للمواد الخام وظروف التفاعل.
استخدامات ثنائي ميثيل أمين
يتمتع DMA بمجموعة واسعة من التطبيقات في مختلف الصناعات نظرًا لخصائصه الكيميائية الفريدة. فيما يلي بعض الاستخدامات الشائعة لـ DMA:
- الصناعة الزراعية: تستخدم مبيدات الأعشاب والمبيدات الحشرية ومبيدات الفطريات المختلفة DEA كوسيط في إنتاجها.
- المستحضرات الصيدلانية: تستخدم كمادة خام لتركيب الأدوية المختلفة، بما في ذلك أدوية التخدير الموضعي والمضادات الحيوية ومضادات الهيستامين.
- صناعة المطاط: يستخدم كمسرع الفلكنة في صناعة المطاط، مما يحسن الخواص الفيزيائية للمنتجات المطاطية.
- صناعة البترول: يستخدم كمثبط للتآكل وعامل تحييد في تكرير البترول.
- معالجة المياه: يستخدم كمندد في معالجة المياه لإزالة المواد الصلبة العالقة والشوائب الأخرى.
- المذيب: يستخدم كمذيب في إنتاج المواد الكيميائية المختلفة، بما في ذلك الراتنجات والأصباغ والبلاستيك.
- صناعة النسيج: يستخدم كمادة صباغة وسيطة وعامل تشطيب في صناعة النسيج.
- العناية الشخصية: يستخدم أيضاً كمكون في منتجات العناية الشخصية المختلفة، بما في ذلك الشامبو والبلسم، حيث يعمل كمعدل لدرجة الحموضة.
أسئلة:
س: أي مما يلي يمثل المعادلة الكاملة للثنائي ميثيل أمين؟
ج: يحدث التعادل الكامل لـ DMA عندما يتفاعل مع حمض الهيدروكلوريك لتكوين كلوريد ثنائي ميثيل الأمونيوم والماء.
س: ما نوع المنتج الذي يحدث عندما يتفاعل 3-بنتانون مع ثنائي ميثيل أمين؟
ج: عندما يتفاعل 3-بنتانون مع DMA، يكون المنتج الناتج إيمين.
س: هل ثنائي ميثيل أمين آمن للشعر؟
ج: يستخدم DMA بشكل شائع في منتجات العناية بالشعر كضابط لدرجة الحموضة ويعتبر آمنًا للاستخدام بتركيزات منخفضة.
س: هل ثنائي ميثيل أمين مفيد للشعر؟
ج: يمكن أن يفيد DMA الشعر عند استخدامه في منتجات العناية بالشعر بتركيزات مناسبة، حيث يمكن أن يساعد في تحسين فعالية المكونات الأخرى.
س: ما هو ثنائي ميثيل أمين؟
ج: DMA مركب عضوي له الصيغة الكيميائية (CH3)2NH. وهو غاز عديم اللون ذو رائحة قوية، ويستخدم عادة في العمليات الصناعية المختلفة.
س: هل يعتمد على ثنائي ميثيل أمين؟
ج: يعتبر DMA قاعدة ضعيفة لأنه يمكنه قبول بروتون من جزيء الماء لتكوين أيون هيدروكسيد وأيون ميثيل الأمونيوم.
س: هل ثنائي ميثيل أمين السيتريل فتاة مجعدة؟
ج: لا يعتبر Cetearyl DMA معتمدًا للفتيات المجعدات، لأنه مكون صناعي شائع الاستخدام في منتجات العناية بالشعر وقد لا يكون مناسبًا لأولئك الذين يتبعون طريقة الفتاة المجعدة.
س: كيف يمكنني العثور على pka من ثنائي ميثيل أمين؟
ج: يمكن العثور على pKa لـ DMA تجريبيًا عن طريق قياس الرقم الهيدروجيني لمحلول ذي تركيز معروف لـ DMA والحمض المرافق له، واستخدام معادلة Henderson-Hasselbalch لحساب قيمة pKa.
س: كيف يمكنك تحضير 100 مل من المخزن المؤقت بدرجة حموضة 11.0 من ثنائي ميثيل أمين؟
ج: لتحضير مخزن مؤقت بدرجة حموضة تبلغ 11.0 من DMA، سيحتاج المرء إلى خلط كمية معينة من DMA مع حمضه المترافق، كلوريد ثنائي ميثيل الأمونيوم، بنسبة محددة لتحقيق الرقم الهيدروجيني المطلوب. ستعتمد الكميات الدقيقة على سعة المخزن المؤقت المطلوبة وpKa للحمض المرافق.
