ثنائي كرومات البوتاسيوم هو مركب كيميائي برتقالي لامع يستخدم في مجموعة متنوعة من التطبيقات. وهو عامل مؤكسد قوي ويمكن أن يكون سامًا إذا تم تناوله أو استنشاقه.
| اسم الأيوباك | ثنائي كرومات البوتاسيوم |
| الصيغة الجزيئية | K2Cr2O7 |
| CAS رقم | 7778-50-9 |
| المرادفات | ثنائي كرومات البوتاسيوم، كرومات البوتاسيوم (VI)، ثنائي كرومات البوتاس |
| إنتشي | InChI=1S/2Cr.2K.7O/q;;2*+1;;;;;;/h;;2*;7*1- |
خصائص ثنائي كرومات البوتاسيوم
صيغة ثنائي كرومات البوتاسيوم
صيغة ثنائي كرومات البوتاسيوم هي K2Cr2O7. ويتكون من ذرتين من البوتاسيوم (K) وذرتين من الكروم (Cr) وسبع ذرات من الأكسجين (O). تحتوي كل ذرة بوتاسيوم على شحنة +1، بينما تحتوي كل ذرة كروم على شحنة +6. يشير وجود ذرتين من الكروم في الصيغة إلى التركيب الثنائي للمركب.
ثنائي كرومات البوتاسيوم الكتلة المولية
يتم حساب الكتلة المولية لثنائي كرومات البوتاسيوم عن طريق إضافة الكتل الذرية للعناصر المكونة له. يحتوي البوتاسيوم على كتلة مولية قدرها 39.10 جرامًا لكل مول (جم / مول)، والكروم لديه كتلة مولية قدرها 52.00 جم / مول، والأكسجين له كتلة مولية قدرها 16.00 جم / مول. وبالتالي فإن الكتلة المولية لثاني كرومات البوتاسيوم هي 294.18 جم / مول.
نقطة غليان ثنائي كرومات البوتاسيوم
ليس لثنائي كرومات البوتاسيوم درجة غليان محددة، فهو يتحلل قبل الوصول إلى درجة الغليان. ومع ذلك، عند تسخينه، فإنه يخضع للتحلل الحراري، مما يؤدي إلى إطلاق أبخرة سامة من أكسيد الكروم والأكسجين.
نقطة انصهار ثنائي كرومات البوتاسيوم
تبلغ نقطة انصهار ثاني كرومات البوتاسيوم حوالي 398 درجة مئوية (درجة مئوية) أو 748 درجة فهرنهايت (درجة فهرنهايت). عند درجة الحرارة هذه، تتحول بلورات ثاني كرومات البوتاسيوم الصلبة إلى الحالة السائلة.
كثافة ثاني كرومات البوتاسيوم جم/مل
تبلغ كثافة ثاني كرومات البوتاسيوم حوالي 2.68 جرام لكل ملليلتر (جم / مل). يشير هذا إلى أن حجمًا معينًا من ثاني كرومات البوتاسيوم أثقل نسبيًا من حجم مساوٍ له من الماء.
الوزن الجزيئي لثنائي كرومات البوتاسيوم
الوزن الجزيئي لثنائي كرومات البوتاسيوم هو نفس الكتلة المولية، وهي 294.18 جرام لكل مول (جم/مول). وهو يمثل الكتلة المجمعة لجميع الذرات الموجودة في جزيء المركب.
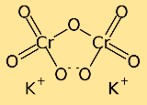
هيكل ثنائي كرومات البوتاسيوم
يحتوي ثنائي كرومات البوتاسيوم على بنية ثنائية اللون، مما يعني أنه يتكون من ذرتين من الكروم مرتبطتين ببعضهما بواسطة ذرات الأكسجين. ترتبط ذرات البوتاسيوم أيضًا بذرات الأكسجين، مما يؤدي إلى إنشاء شبكة معقدة من الذرات في المركب.
ذوبان ثاني كرومات البوتاسيوم
ثنائي كرومات البوتاسيوم قابل للذوبان بشدة في الماء. يذوب بسهولة في الماء ليشكل محلول برتقالي. تزداد ذوبان ثاني كرومات البوتاسيوم مع درجة الحرارة. ومع ذلك، فإن قابليته للذوبان في المذيبات العضوية محدودة.
| مظهر | بلورات برتقالية زاهية |
| جاذبية معينة | 2.68 جرام/مل |
| لون | البرتقالي |
| يشم | عديم الرائحة |
| الكتلة المولية | 294.18 جرام/مول |
| كثافة | 2.68 جرام/مل |
| نقطة الانصهار | 398 درجة مئوية (748 درجة فهرنهايت) |
| نقطة الغليان | متحللة |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | قابل للذوبان للغاية |
| الذوبان | قابل للذوبان في الماء، محدودة في المذيبات العضوية |
| ضغط البخار | ضئيلة |
| كثافة بخار | غير متاح |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | حمضية (حوالي الرقم الهيدروجيني 4) |
سلامة ومخاطر ثنائي كرومات البوتاسيوم
يشكل ثاني كرومات البوتاسيوم مخاطر كبيرة على السلامة. وهو شديد السمية إذا تم تناوله أو استنشاقه أو ملامسته للجلد. المركب عبارة عن عامل مؤكسد قوي يمكن أن يتفاعل بعنف مع المواد القابلة للاحتراق، مما يزيد من خطر نشوب حريق. التعرض لثنائي كرومات البوتاسيوم يمكن أن يسبب تهيجًا شديدًا في الجلد وحروقًا وتفاعلات حساسية. استنشاق أبخرة أو غبارها يمكن أن يسبب مشاكل في الجهاز التنفسي وتلف الرئة. ويرتبط التعرض طويل الأمد بآثار صحية ضارة، بما في ذلك سرطان الرئة الناجم عن الكرومات. من الضروري التعامل مع ثنائي كرومات البوتاسيوم بحذر شديد، وارتداء معدات الحماية المناسبة وضمان التهوية الكافية لتقليل مخاطر الصحة والسلامة.
| رموز الخطر | تآكل، خطر على الصحة، سامة حادة |
| وصف الأمان | – شديد السمية – مسبب للتآكل – يسبب الحروق |
| أرقام تعريف الأمم المتحدة | رقم الأمم المتحدة 3086 (الفئة 6.1) |
| رمز النظام المنسق | 2841.10.10 |
| فئة الخطر | 6.1 (المواد السامة) |
| مجموعة التعبئة | ثالثا |
| تسمم | السمية الفموية الحادة: شديدة السمية<br>السمية المزمنة: احتمالية الإصابة بالسرطان |
ملحوظة: رموز الخطر المستخدمة في الجدول هي رموز دولية معترف بها بشكل عام. من المهم الرجوع إلى اللوائح المحددة وتعليمات السلامة للحصول على معلومات كاملة حول التعامل مع ثاني كرومات البوتاسيوم وتخزينه.
طرق تصنيع ثنائي كرومات البوتاسيوم
هناك عدة طرق لتصنيع ثنائي كرومات البوتاسيوم. تتضمن الطريقة الشائعة التفاعل بين كرومات البوتاسيوم (K2CrO4) وحمض الكروميك (H2CrO4) . يحدث التفاعل في بيئة حمضية، عادة باستخدام حمض الكبريتيك (H2SO4) كمحفز. يمكن تلخيص رد الفعل.
2K2CrO4 + 2H2CrO4 + 2H2SO4 → K2Cr2O7 + Cr2(SO4)3 + 4H2O
تتضمن الطريقة الأخرى أكسدة كرومات البوتاسيوم باستخدام عامل مؤكسد قوي، مثل حمض الكبريتيك المركز (H2SO4) ، وعامل اختزال، مثل الإيثانول (C2H5OH). يمكن تلخيص رد الفعل.
2K2CrO4 + H2SO4 + 3C2H5OH → K2Cr2O7 + Cr2(SO4)3 + 7H2O + 3CO2
يتفاعل هيدروكسيد البوتاسيوم (KOH) مع ثالث أكسيد الكروم (CrO3) في وسط مائي لإنتاج ثاني كرومات البوتاسيوم. في وسط مائي، يحدث التفاعل. يمكن تلخيص رد الفعل.
2KOH + CrO3 → K2Cr2O7 + H2O
تتطلب طرق التوليف هذه احتياطات السلامة المناسبة بسبب الطبيعة السامة والمسببة للتآكل للكواشف المعنية. من المهم إجراء هذه التفاعلات في منطقة جيدة التهوية، وارتداء معدات الحماية، والتعامل مع المواد الكيميائية بعناية. بالإضافة إلى ذلك، يعد اتباع البروتوكولات المناسبة للتخلص من النفايات أمرًا ضروريًا لتقليل التأثير البيئي.
استخدامات ثنائي كرومات البوتاسيوم
يجد ثنائي كرومات البوتاسيوم تطبيقات في مختلف المجالات بسبب خصائصه الفريدة. فيما يلي بعض استخداماته الشائعة:
- عامل مؤكسد: تستخدم التفاعلات الكيميائية على نطاق واسع ثنائي كرومات البوتاسيوم كعامل مؤكسد قوي لأكسدة الكحولات إلى الألدهيدات أو الكيتونات.
- الكاشف المعملي: تستخدم الكيمياء التحليلية ثاني كرومات البوتاسيوم ككاشف للاختبارات والتجارب، بما في ذلك تحديد المركبات العضوية وإجراء تفاعلات الأكسدة والاختزال.
- صناعة الدباغة: تستخدم صناعة الجلود ثاني كرومات البوتاسيوم كعامل دباغة لمعالجة جلود الحيوانات وتحويلها إلى منتجات جلدية متينة.
- التصوير الفوتوغرافي: يدمج التصوير الفوتوغرافي بالأبيض والأسود ثنائي كرومات البوتاسيوم في المحاليل النامية ويستخدمه لتوعية المستحلبات لتحقيق تأثيرات فوتوغرافية محددة.
- الحفاظ على الخشب: لحماية الخشب من التعفن والفطريات وهجمات الحشرات، تستخدم صناعة حفظ الأخشاب ثاني كرومات البوتاسيوم كمادة حافظة للخشب شديدة السمية.
- صناعة الأصباغ: يلعب ثنائي كرومات البوتاسيوم دوراً حيوياً في إنتاج الأصباغ مثل الكروم الأصفر والكروم البرتقالي، والتي تستخدمها الصناعات في صناعة الدهانات والأحبار والأصباغ.
- الطلاء الكهربائي: تستخدم عمليات الطلاء الكهربائي ثنائي كرومات البوتاسيوم لتوفير طلاء زخرفي مقاوم للتآكل على المعادن بما في ذلك الزنك والألومنيوم والنحاس.
- الألعاب النارية: يلعب ثاني كرومات البوتاسيوم دورًا أساسيًا في مخاليط الألعاب النارية، حيث يوفر ألوانًا برتقالية زاهية للألعاب النارية والمشاعل.
- صناعة النسيج: تتضمن صباغة وطباعة المنسوجات ثنائي كرومات البوتاسيوم لتحقيق الألوان المطلوبة وتحسين ثبات اللون.
- معايرة الأواني الزجاجية للمختبر: للحصول على قياسات دقيقة للحجم، يتم استخدام محاليل ثاني كرومات البوتاسيوم لمعايرة الأواني الزجاجية للمختبر.
تسلط هذه التطبيقات المتنوعة الضوء على تنوع وأهمية ثنائي كرومات البوتاسيوم في مختلف الصناعات والمساعي العلمية.
أسئلة:
س: ما هي الصيغة الصحيحة لثنائي كرومات البوتاسيوم؟
ج: الصيغة الصحيحة لثنائي كرومات البوتاسيوم هي K2Cr2O7.
س: ما هو ثنائي كرومات البوتاسيوم؟
ج: ثنائي كرومات البوتاسيوم مركب كيميائي برتقالي اللون ويشيع استخدامه كعامل مؤكسد.
س: هل ثنائي كرومات البوتاسيوم أيوني أم تساهمي؟
ج: ثنائي كرومات البوتاسيوم مركب أيوني.
س: ما هو الحد الأدنى من الماء اللازم لإذابة 3 مولات من ثنائي كرومات البوتاسيوم؟
ج: أقل كمية من الماء اللازمة لإذابة 3 مولات من ثاني كرومات البوتاسيوم هي 564 جرام تقريبًا.
س: ما هي الكتلة المولية لثاني كرومات البوتاسيوم؟
ج: الكتلة المولية لثاني كرومات البوتاسيوم هي 294.18 جرام لكل مول (جم/مول).
س: ثاني كرومات البوتاسيوم MSDS؟
ج: توفر صحائف بيانات سلامة المواد (MSDS) الخاصة بثاني كرومات البوتاسيوم معلومات تفصيلية عن مخاطرها ومعالجتها وتخزينها وإجراءات الإسعافات الأولية. يرجى الرجوع إلى المصادر أو الشركات المصنعة الموثوقة للحصول على صحيفة بيانات سلامة المواد (MSDS) المحددة.
س: كيف يتم تحضير ثنائي كرومات البوتاسيوم من خام الكروميت؟
ج: يمكن تحضير ثنائي كرومات البوتاسيوم من خام الكروميت عن طريق تحميصه مع هيدروكسيد البوتاسيوم أو كربونات البوتاسيوم ومن ثم عزل المنتج.
س: ما عدد جرامات ثاني كرومات البوتاسيوم التي أضيفت إلى الدورق الحجمي؟
ج: يعتمد العدد الدقيق لجرامات ثاني كرومات البوتاسيوم المضافة إلى الدورق الحجمي على التركيز المطلوب وحجم المحلول.
س: كيف يمكنك التمييز بين البروبانال والبروبانون باستخدام ثنائي كرومات البوتاسيوم المحمض؟
ج: سوف يتأكسد البروبانال إلى حمض البروبانويك بواسطة ثنائي كرومات البوتاسيوم المحمض، في حين أن البروبانون (الأسيتون) لن يظهر أي تفاعل.
س: هل ثنائي كرومات البوتاسيوم عامل اختزال؟
ج: لا، ثنائي كرومات البوتاسيوم عامل مؤكسد.
س: كيف تكتب صيغة ثاني كرومات البوتاسيوم؟
ج: صيغة ثاني كرومات البوتاسيوم هي K2Cr2O7.
