ثاني كلوريد الكبريت (SCl₂) هو مركب كيميائي يتكون من الجمع بين الكبريت والكلور. يتم استخدامه في الصناعات المختلفة لصنع الأصباغ والمطاط والمبيدات الحشرية.
| اسم الأيوباك | ثنائي كلوريد الكبريت |
| الصيغة الجزيئية | SCl₂ |
| CAS رقم | 10545-99-0 |
| المرادفات | أحادي كبريتيد الكلور، كلوريد الكبريت، ثنائي كلوريد الكبريت، كلوريد الكبريت، ثنائي كلورو سلفان |
| إنتشي | إنتشي = 1S/Cl2S/c1-3-2 |
خصائص ثاني كلوريد الكبريت
صيغة ثاني كلوريد الكبريت
صيغة كلوريد الكبريت هي SCl₂. وهو يمثل مزيجًا من ذرة كبريت واحدة وذرتين من الكلور. تعكس هذه الصيغة الكيميائية بدقة تركيبة المركب وبنيته.
ثاني كلوريد الكبريت الكتلة المولية
يمكن حساب الكتلة المولية لكلوريد الكبريت عن طريق إضافة الكتل الذرية للعناصر المكونة له. يحتوي الكبريت على كتلة مولية قدرها 32.06 جم/مول، بينما تبلغ الكتلة المولية للكلور 35.45 جم/مول. وبإضافة كتلتي ذرتي كلور وذرة كبريت واحدة، يتم تحديد الكتلة المولية لكلوريد الكبريت بحوالي 102.91 جم/مول.
نقطة غليان ثاني كلوريد الكبريت
كلوريد الكبريت لديه نقطة غليان تبلغ 138.8 درجة مئوية (281.8 درجة فهرنهايت). تشير درجة الحرارة هذه إلى النقطة التي يتحول عندها المركب السائل إلى الحالة الغازية تحت الضغط الجوي القياسي. من المهم مراعاة درجة غليان كلوريد الكبريت عند التعامل معه أو استخدامه في التطبيقات المختلفة.
نقطة انصهار ثنائي كلوريد الكبريت
نقطة انصهار كلوريد الكبريت هي -76.8 درجة مئوية (-106.2 درجة فهرنهايت). تمثل درجة الحرارة هذه النقطة التي يتحول عندها المركب الصلب إلى الحالة السائلة. تعد معرفة نقطة الانصهار أمرًا ضروريًا عند العمل مع كلوريد الكبريت لضمان المعالجة والتخزين المناسبين.
كثافة ثاني كلوريد الكبريت جم/مل
تبلغ كثافة كلوريد الكبريت حوالي 1.64 جم / مل. تشير قيمة الكثافة إلى مقدار الكتلة لكل وحدة حجم المادة. هذه الخاصية ضرورية لفهم سلوك وخصائص كلوريد الكبريت في سياقات مختلفة، مثل أثناء التفاعلات الكيميائية أو لتحديد مدى ملاءمتها لتطبيقات محددة.
الوزن الجزيئي لثاني كلوريد الكبريت
يبلغ الوزن الجزيئي لكلوريد الكبريت حوالي 102.91 جم / مول. وهو يمثل الكتلة الإجمالية لجزيء المركب، ويتم حسابها عن طريق إضافة الكتل الذرية للعناصر المكونة له. يوفر الوزن الجزيئي معلومات قيمة عن كتلة المركب ويسمح بإجراء قياسات دقيقة في الحسابات الكيميائية المختلفة.
هيكل ثاني كلوريد الكبريت
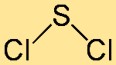
من الأفضل وصف بنية كلوريد الكبريت على أنها جزيء منحني أو على شكل حرف V. وتتكون من ذرة كبريت مركزية مرتبطة بذرتين من الكلور. يساهم ترتيب الذرات وزوايا روابطها في الاستقرار العام وتفاعلية المركب.
ذوبان ثاني كلوريد الكبريت
كلوريد الكبريت محدود الذوبان في الماء. وهو ضعيف الذوبان ويميل إلى تكوين محلول غائم عند مزجه بالماء. من المهم أخذ خصائص ذوبان المركب في الاعتبار عند تحديد مدى توافقه مع المواد الأخرى وسلوكه في المذيبات المختلفة.
| مظهر | سائل أصفر |
| جاذبية معينة | 1.64 جم/مل |
| لون | أصفر |
| يشم | فدان |
| الكتلة المولية | 102.91 جم/مول |
| كثافة | 1.64 جم/مل |
| نقطة الانصهار | -76.8 درجة مئوية |
| نقطة الغليان | 138.8 درجة مئوية |
| نقطة فلاش | غير متاح |
| الذوبان في الماء | يتفاعل |
| الذوبان | قابل للذوبان في حمض الخليك الجليدي والبنزين والبروم |
| ضغط البخار | 35.4 ملم زئبق |
| كثافة بخار | 3.9 (الهواء=1) |
| pKa | غير متاح |
| الرقم الهيدروجيني | غير متاح |
السلامة ومخاطر ثاني كلوريد الكبريت
يشكل كلوريد الكبريت العديد من مخاطر السلامة ويجب التعامل معه بحذر. وهو شديد التآكل ويمكن أن يسبب حروقًا شديدة عند ملامسته للجلد أو العينين أو الأغشية المخاطية. استنشاق أبخرته قد يهيج الجهاز التنفسي ويسبب السعال وصعوبة التنفس وتلف الرئة. كما أنه قابل للاشتعال ويمكن أن يشتعل في وجود مواد معينة. عند العمل مع كلوريد الكبريت، يجب استخدام معدات الحماية المناسبة مثل القفازات والنظارات الواقية وحماية الجهاز التنفسي. ومن الضروري التعامل مع هذا المركب وتخزينه في منطقة جيدة التهوية، بعيدًا عن مصادر الاشتعال والمواد غير المتوافقة، لتجنب الحوادث والأضرار المحتملة.
| رموز الخطر | تآكل |
| وصف الأمان | تجنب الاتصال وارتداء معدات الحماية والعمل في مناطق جيدة التهوية |
| أرقام تعريف الأمم المتحدة | أ 1828 |
| رمز النظام المنسق | 2812.10.00 |
| فئة الخطر | 8 (المواد المسببة للتآكل) |
| مجموعة التعبئة | ثانيا |
| تسمم | سام جدا |
طرق تصنيع ثاني كلوريد الكبريت
هناك عدة طرق لتجميع كلوريد الكبريت. يتضمن النهج الشائع التفاعل بين غاز الكبريت والكلور. في هذه العملية، يوجد الكلور الزائد عند تسخين الكبريت إلى درجة حرارة معينة، عادة حوالي 200-250 درجة مئوية (392-482 درجة فهرنهايت). يستمر التفاعل لتكوين كلوريد الكبريت.
تتضمن الطريقة الأخرى التفاعل بين كلوريد الثيونيل (SOCl₂) والكبريت. يعمل كلوريد الثيونيل كمصدر للكلور، الذي يتفاعل مع الكبريت لإنتاج كلوريد الكبريت. يحدث هذا التفاعل عند درجة حرارة أقل نسبيًا من طريقة الكبريت المباشر.
التفاعل بين كلوريد السلفوريل (SO₂Cl₂) وكبريتيد الهيدروجين (H₂S) يسمح بتحضير كلوريد الكبريت. يحدث هذا التفاعل عند درجات حرارة عالية وينتج كلوريد الكبريت ومنتجات ثانوية أخرى.
لضمان سلامة الموظفين المشاركين، من الأهمية بمكان إجراء تخليق كلوريد الكبريت في مختبرات مجهزة تجهيزا جيدا أو البيئات الصناعية. يجب على الموظفين اتباع احتياطات السلامة المناسبة، بما في ذلك ارتداء معدات الحماية والعمل في مناطق جيدة التهوية، وذلك بسبب الطبيعة الخطرة للمجمع.
يعتمد اختيار طريقة التوليف على عوامل مختلفة، بما في ذلك توافر المواد الخام، والنقاء المطلوب للمنتج، ومتطلبات التطبيق المحددة. ويعتمد اختيار التقنية المناسبة على الاحتياجات المحددة للعملية أو التطبيق، حيث أن كل طريقة لها مزاياها واعتباراتها الخاصة.
استخدامات ثاني كلوريد الكبريت
يجد كلوريد الكبريت (SCl₂) تطبيقات في مختلف الصناعات والعمليات نظرًا لخصائصه المحددة. فيما يلي بعض الاستخدامات الرئيسية لكلوريد الكبريت:
- تصنيع الأصباغ: يستخدم المصنعون كلوريد الكبريت لإنتاج الأصباغ، وخاصة الأصباغ الكبريتية، التي تضفي ألوانًا نابضة بالحياة على الأقمشة في صناعة النسيج.
- صناعة المطاط: تستخدم صناعة المطاط SCl₂ كعامل فلكنة لتحسين قوة ومرونة المنتجات المطاطية عن طريق ربط سلاسل البوليمر.
- تخليق المبيدات الحشرية: يلعب كلوريد الكبريت دورًا حاسمًا في تصنيع بعض المبيدات الحشرية، مما يتيح إنتاج المبيدات الحشرية ومبيدات الفطريات التي تسمى مركبات الفوسفات العضوية والفوسفات العضوية.
- التخليق الكيميائي: يعمل SCl₂ ككاشف متعدد الاستخدامات في التفاعلات الكيميائية المختلفة، مما يتيح تفاعلات الكلورة مثل تحويل الكحولات إلى كلوريدات الألكيل أو تخليق المركبات العضوية المكلورة.
- كاشف المختبر: تستخدم المختبرات كلوريد الكبريت ككاشف لتطبيقات متعددة، بما في ذلك التخليق العضوي، وكيمياء الكبريت، والتفاعلات غير العضوية.
- معالجة المياه: تستخدم عمليات معالجة المياه SCl₂ كعامل مطهر ومؤكسد لإزالة الكائنات الحية الدقيقة الضارة والملوثات العضوية من مصادر المياه.
- صناعة المستحضرات الصيدلانية: يجد كلوريد الكبريت تطبيقات في البحث والتطوير الصيدلاني، وخاصة في تركيب بعض المكونات الصيدلانية النشطة (API).
- التحليل الكيميائي: تستخدم تقنيات الكيمياء التحليلية، مثل كروماتوغرافيا الغاز، SCl₂ للكشف عن مركبات معينة وتحليلها.
تسلط هذه التطبيقات المختلفة الضوء على أهمية كلوريد الكبريت في مختلف العمليات الصناعية والمساعي العلمية. ومع ذلك، من المهم التعامل مع كلوريد الكبريت واستخدامه بعناية، مع اتباع إرشادات وإجراءات السلامة المناسبة بسبب طبيعته الخطرة.
أسئلة:
س: ما هي صيغة ثنائي كلوريد الكبريت؟
ج: صيغة كلوريد الكبريت هي SCl₂.
س: ما الصيغة التي تمثل المركب الجزيئي ثنائي كلوريد الكبريت؟
ج: يتم تمثيل المركب الجزيئي كلوريد الكبريت بالصيغة SCl₂.
س: هل ثنائي كلوريد الكبريت قطبي؟
ج: نعم، كلوريد الكبريت قطبي بسبب وجود هندسة جزيئية منحنية وتوزيع غير متساوي لكثافة الإلكترون.
س: ما هي المدارات الذرية أو الهجينة التي تشكل رابطة سيجما بين S وCl في ثاني كلوريد الكبريت، SCl₂؟
ج: تتكون رابطة سيجما بين الكبريت (S) والكلور (Cl) في كلوريد الكبريت (SCl₂) من خلال تداخل المدار 3p للكبريت والمدار 3p للكلور.
س: هل SCl₂ خطي؟
ج: لا، كلوريد الكبريت (SCl₂) ليس خطيًا. لها هندسة جزيئية منحنية أو على شكل حرف V.
س: أي مما يلي مركب أيوني؟ Cl₂O، CH₂O، SCl₂، PF₅، Mg₃(PO₄)₂.
ج: لا يعتبر أي من المركبات المذكورة مركبات أيونية. وهي إما مركبات جزيئية (Cl₂O، CH₂O، SCl₂، PF₅) أو مركب فوسفات غير عضوي (Mg₃(PO₄)₂).
س: ما اسم المركب الذي صيغته SCl₂؟
ج: المركب الذي له الصيغة SCl₂ يسمى كلوريد الكبريت.
س: ما هو شكل SCl₂؟
ج: يحتوي SCl₂ على شكل جزيئي منحني أو على شكل حرف V.
س: ما هي الهندسة الجزيئية لـ SCl₂؟
ج: الهندسة الجزيئية لـ SCl₂ منحنية أو على شكل حرف V.
س: ما أسماء المدارات الهجينة التي يستخدمها الكبريت في SCl₂؟
ج: تستخدم ذرة الكبريت في SCl₂ مدارات هجينة sp².
س: ماذا يحدث عندما تتحد ذرة كبريت مع ذرتين من الكلور لتكوين SCl₂؟
ج: عندما تتحد ذرة كبريت واحدة مع ذرتين من الكلور لتكوين المركب SCl₂، المعروف بكلوريد الكبريت. تتشارك ذرة الكبريت الإلكترونات مع ذرات الكلور لتكوين رابطة تساهمية بينهما.
