بروميد البوتاسيوم (KBr) هو مركب كيميائي يتكون من البوتاسيوم والبروم. يستخدم عادة في التصوير الفوتوغرافي والطب والطب البيطري كمضاد للاختلاج للكلاب.
| اسم الأيوباك | بروميد البوتاسيوم |
| الصيغة الجزيئية | KBr |
| CAS رقم | 7758-02-3 |
| المرادفات | بروميد البوتاسيوم، ملح بروميد البوتاسيوم، كاليوبروميد، بروموبوتاسيوم |
| إنتشي | InChI=1S/BrH.K/h1H;/q;+1/p-1 |
خصائص بروميد البوتاسيوم
صيغة بروميد البوتاسيوم
الصيغة الكيميائية لبروميد البوتاسيوم هي KBr. تمثل هذه الصيغة نسبة الذرات في المركب. يحتوي أيون K+ على شحنة +1، بينما يحمل أيون البريون شحنة -1، مما ينتج عنه مركب متعادل. تُستخدم الصيغة للإشارة إلى تركيب المركب وهي ضرورية لكتابة المعادلات الكيميائية الموزونة.
بروميد البوتاسيوم الكتلة المولية
يمتلك KBr كتلة مولية تبلغ 119.01 جم/مول. وتتكون من ذرة بوتاسيوم واحدة وذرة بروم واحدة. تعد الكتلة المولية خاصية مهمة للمركب لأنها تستخدم لتحديد عدد مولات المادة في عينة معينة. كما أنها تستخدم في قياس العناصر الكيميائية لحساب كتلة المنتج أو المادة المتفاعلة في التفاعل الكيميائي.
نقطة غليان بروميد البوتاسيوم
تبلغ درجة غليان KBr 1,390 درجة مئوية (2,534 درجة فهرنهايت). ترجع نقطة الغليان العالية هذه إلى الطبيعة الأيونية للمركب. عند تسخينها، تتطلب الروابط الأيونية بين البوتاسيوم والبروم كمية كبيرة من الطاقة لكسرها، مما يؤدي إلى ارتفاع درجة الغليان. يستخدم KBr بشكل شائع في المختبر كسائل نقل الحرارة بسبب نقطة غليانه العالية.
بروميد البوتاسيوم نقطة الانصهار
لدى KBr نقطة انصهار تبلغ 734 درجة مئوية (1353 درجة فهرنهايت). تمامًا مثل نقطة الغليان، يتم تحديد نقطة الانصهار أيضًا من خلال قوة الروابط الأيونية بين ذرات البوتاسيوم والبروم. عند تسخينها، تضعف الروابط الأيونية وينهار هيكل الشبكة البلورية للمركب، مما يؤدي إلى الحالة السائلة.
كثافة بروميد البوتاسيوم جم/مل
تبلغ كثافة KBr 2.75 جم/مل عند درجة حرارة الغرفة. يتم تعريف كثافة المادة على أنها كتلة المادة لكل وحدة حجم. ترجع الكثافة العالية لـ KBr إلى التركيب البلوري الضيق للمركب. هذه الخاصية تجعله مفيدًا في صنع المواد البصرية مثل العدسات والمنشورات.
بروميد البوتاسيوم الوزن الجزيئي
الوزن الجزيئي لـ KBr هو 119.01 جم/مول. يتم حساب هذه القيمة عن طريق إضافة الكتل الذرية للبوتاسيوم والبروم. ويستخدم الوزن الجزيئي في الحسابات الكيميائية مثل تحديد كمية المادة اللازمة لتحضير محلول بتركيز معين.
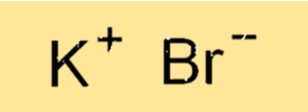
هيكل بروميد البوتاسيوم
يحتوي KBr على بنية بلورية تتكون من شبكة مكعبة مركزية الوجه. كل أيون K+ محاط بستة أيونات من البريونات، وكل بريون محاط بستة أيونات K+. وهذا الترتيب هو سمة من سمات المركبات الأيونية، التي لها ترتيب منتظم ومتكرر للأيونات في البنية البلورية.
| مظهر | مادة صلبة بلورية بيضاء |
| جاذبية معينة | 2.75 جم/مل عند 25 درجة مئوية |
| لون | عديم اللون |
| يشم | عديم الرائحة |
| الكتلة المولية | 119.01 جم/مول |
| كثافة | 2.75 جم/سم3 |
| نقطة الانصهار | 734 درجة مئوية (1,353 درجة فهرنهايت) |
| نقطة الغليان | 1390 درجة مئوية (2534 درجة فهرنهايت) |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | 53 جم/100 مل عند 20 درجة مئوية |
| الذوبان | قابل للذوبان في الكحول والأسيتون والأمونيا |
| ضغط البخار | 1 ملم زئبق عند 1114 درجة مئوية |
| كثافة بخار | غير قابل للتطبيق |
| pKa | 7.5 (عند 25 درجة مئوية) |
| الرقم الهيدروجيني | 7 (محايد) |
سلامة ومخاطر بروميد البوتاسيوم
يعتبر KBr بشكل عام آمنًا للاستخدام، ولكنه قد يشكل بعض المخاطر إذا تم التعامل معه بشكل خاطئ. وهو مهيج للجلد والعين والجهاز التنفسي، ويمكن أن يسبب تناوله اضطرابًا في الجهاز الهضمي. التعرض لفترات طويلة لتركيزات عالية قد يسبب مشاكل في الجهاز التنفسي. يجب التعامل مع KBr بعناية ويجب ارتداء معدات الحماية الشخصية المناسبة، بما في ذلك القفازات وقناع الغبار، عند التعامل مع المركب. من المهم أيضًا تخزين KBr في منطقة باردة وجافة وجيدة التهوية بعيدًا عن المواد غير المتوافقة. إذا تعرضت، اطلب العناية الطبية على الفور.
| رموز الخطر | شي – مزعج |
| وصف الأمان | تجنب ملامسة الجلد والعينين. ارتداء الملابس الواقية المناسبة والقفازات والنظارات الواقية / درع الوجه |
| حماية. | |
| أرقام تعريف الأمم المتحدة | رقم الأمم المتحدة 1465 (المواد الكيميائية، بروميد البوتاسيوم) |
| رمز النظام المنسق | 28275100 |
| فئة الخطر | 6.1 (المواد السامة) |
| مجموعة التعبئة | ثالثا |
| تسمم | الجرعة المميتة 50 (عن طريق الفم، الفئران) = 2.340 ملغم/كغم |
طرق تصنيع بروميد البوتاسيوم
لتصنيع KBr، يمكن للمرء استخدام طرق مختلفة مثل التوليف المباشر، والتحلل المزدوج، والمعايرة الحمضية القاعدية.
يتفاعل KOH مع غاز HBr لإنتاج KBr في التوليف المباشر. ينتج عن التفاعل KBr والماء كمنتجات ثانوية.
يتضمن التحلل المزدوج تفاعل ملح البوتاسيوم القابل للذوبان مع ملح بروميد قابل للذوبان، مثل كلوريد البوتاسيوم وبروميد الصوديوم. ينتج عن التفاعل KBr وكلوريد الصوديوم .
تتضمن معايرة الحمض مع القاعدة تفاعل ملح البروميد مع “KOH” . يعالج حمض الكبريتيك المخفف أولاً ملح البروميد لتكوين Hbr، ثم KOH العنوان لإنتاج KBr والماء.
هناك طريقة أخرى لتصنيع KBr تتضمن تفاعل البروم مع محلول ساخن من هيدروكسيد البوتاسيوم . يقلل كبريتيت الصوديوم من برومات البوتاسيوم، وينتج KBr وبرومات البوتاسيوم.
استخدامات بروميد البوتاسيوم
لدى KBr عدة استخدامات في مختلف الصناعات نظرًا لخصائصها الفريدة. فيما يلي بعض الاستخدامات الشائعة لـ KBr:
- التصوير الفوتوغرافي: يستخدم على نطاق واسع في التصوير الفوتوغرافي بالأبيض والأسود كمثبت للصور الفوتوغرافية لمنع تعفير ورق التصوير الفوتوغرافي.
- الطب البيطري: يستخدم كدواء مضاد للتشنجات للكلاب والقطط التي تعاني من النوبات.
- الكيمياء التحليلية: تستخدم كمعيار مرجعي في التحليل الطيفي للأشعة تحت الحمراء لتحويل فورييه (FTIR) لتحديد المركبات العضوية.
- الكيمياء الطبية: تستخدم في تحضير الأدوية المختلفة، بما في ذلك المهدئات، والمنومات، ومضادات الصرع.
- التنقيب عن النفط: يستخدم كمائع استكمال في التنقيب عن النفط لمنع تدفق مياه التكوين وتقليل مخاطر التآكل.
- مثبطات اللهب: تستخدم كمثبطات للهب في البلاستيك والمنسوجات والمنتجات الورقية.
- التخليق الكيميائي: يستخدم أيضًا في تفاعلات التخليق الكيميائي، وخاصة في تركيب المركبات العضوية وغير العضوية المختلفة.
أسئلة:
س: في أي ظروف يمكن لبروميد البوتاسيوم توصيل الكهرباء؟
ج: يستطيع KBr توصيل الكهرباء عندما يكون في حالة منصهرة أو عندما يذوب في الماء، مما يسمح لأيوناته بالتحرك بحرية وحمل شحنة كهربائية.
س: هل KBr أيوني أم تساهمي؟
ج: KBr مركب أيوني يتكون من انتقال الإلكترونات من البوتاسيوم إلى البروم.
س: هل KBr قابل للذوبان في الماء؟
ج: نعم، KBr قابل للذوبان بدرجة عالية في الماء، مع قابلية ذوبان تبلغ 53.5 جم / 100 مل عند 25 درجة مئوية.
س: ما هي صيغة بروميد البوتاسيوم؟
ج: الصيغة الكيميائية لبروميد البوتاسيوم هي KBr.
س: هل KBr حمض أم قاعدة؟
ج: KBr عبارة عن ملح وليس له خصائص حمضية أو قاعدية.
س: ما هو KBr؟
ج: KBr هو الرمز الكيميائي لبروميد البوتاسيوم، وهو مركب أيوني يستخدم في العديد من الصناعات لخصائصه الفريدة.
س: ما مقدار كتلة KBr (بالجرام) التي تحتاجها لتحضير 250.0 مل من محلول 1.50 M KBr؟
ج: لتحضير محلول 1.50 M KBr في 250.0 مل من الماء، سوف تحتاج إلى إذابة 30.4 جرام من KBr في الماء.
