إيثيل بنزين (C8H10) مركب عضوي ذو رائحة حلوة. يتم استخدامه كمذيب في مختلف الصناعات، بما في ذلك البلاستيك والمطاط. ويوجد أيضًا في البنزين ويستخدم في تركيب بعض المنتجات المنزلية.
| اسم الأيوباك | إيثيل بنزين |
| الصيغة الجزيئية | C8H10 |
| CAS رقم | 100-41-4 |
| المرادفات | إيثيلبنزول، EB، فينيل إيثان، إيثيل فينيل، 2-فينيل إيثان، ألفا ميثيل تولوين، 1-فينيل إيثان، إيتيل بنزين، مخفف ستايرين |
| إنتشي | إنشي=1S/C8H10/c1-2-8-6-4-3-5-7-8/h3-7H,2H2,1H3 |
خصائص إيثيل بنزين
صيغة إيثيل بنزين
الصيغة الجزيئية للإيثيل بنزين هي C8H10، مما يعني أنه يتكون من ثماني ذرات كربون وعشر ذرات هيدروجين. يتميز التركيب الكيميائي للإيثيل بنزين بحلقة بنزين متصلة بمجموعة إيثيل.
الكتلة المولية لإيثيل بنزين
الكتلة المولية لـ C8H10 هي 106.17 جم/مول. يتم حساب ذلك عن طريق إضافة الكتل الذرية لجميع الذرات الموجودة في جزيء C8H10.
نقطة غليان إيثيل بنزين
نقطة غليان C8H10 هي 136.2 درجة مئوية (277.2 درجة فهرنهايت). هذه هي درجة الحرارة التي يتحول عندها الشكل السائل لـ C8H10 إلى غاز. يتمتع C8H10 بنقطة غليان منخفضة نسبيًا مقارنة بالهيدروكربونات العطرية الأخرى، مما يجعله مفيدًا كمذيب في مختلف الصناعات.
نقطة انصهار إيثيل بنزين
نقطة انصهار C8H10 هي -95.2 درجة مئوية (-139.4 درجة فهرنهايت). هذه هي درجة الحرارة التي يتحول عندها الشكل الصلب لـ C8H10 إلى سائل. يتمتع C8H10 بنقطة انصهار منخفضة نسبيًا مقارنة بالهيدروكربونات العطرية الأخرى، مما يجعله مفيدًا كمادة خام لإنتاج مواد كيميائية أخرى.
كثافة إيثيل بنزين جم / مل
تبلغ كثافة C8H10 0.867 جم / مل عند 20 درجة مئوية (68 درجة فهرنهايت). وهذا يعني أن الملليلتر الواحد من C8H10 يزن 0.867 جرام عند درجة الحرارة هذه. C8H10 أقل كثافة من الماء، مما يعني أنه سوف يطفو على سطح الماء إذا تم خلط السائلين.
الوزن الجزيئي لإيثيل بنزين
الوزن الجزيئي لـ C8H10 هو 106.17 جم/مول. هذه هي كتلة جزيء C8H10، والتي يمكن حسابها عن طريق إضافة الكتل الذرية لجميع الذرات الموجودة في الجزيء.
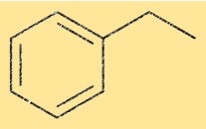
هيكل إيثيل بنزين
يتكون هيكل C8H10 من حلقة بنزين متصلة بمجموعة إيثيل. ترتبط مجموعة الإيثيل بإحدى ذرات الكربون في حلقة البنزين. يُعرف هذا الهيكل أيضًا باسم فينيل إيثان.
ذوبان إيثيل بنزين
C8H10 غير قابل للذوبان في الماء ولكنه قابل للذوبان في المذيبات العضوية مثل الكحول والإيثرات والكلوروفورم. وهذا يعني أن C8H10 لن يذوب في الماء، ولكنه سوف يذوب في سوائل أخرى لها خصائص كيميائية مماثلة. تعتمد قابلية ذوبان C8H10 في المذيبات المختلفة على عوامل مثل درجة الحرارة والضغط والخواص الكيميائية للمذيب.
| مظهر | سائل عديم اللون |
| جاذبية معينة | 0.867 جم/مل عند 20 درجة مئوية |
| لون | عديم اللون |
| يشم | رائحة حلوة |
| الكتلة المولية | 106.17 جرام/مول |
| كثافة | 0.867 جم/مل عند 20 درجة مئوية |
| نقطة الانصهار | -95.2 درجة مئوية (-139.4 درجة فهرنهايت) |
| نقطة الغليان | 136.2 درجة مئوية (277.2 درجة فهرنهايت) |
| نقطة فلاش | 11.1 درجة مئوية (52 درجة فهرنهايت) |
| الذوبان في الماء | 0.30 جم/لتر عند 20 درجة مئوية |
| الذوبان | قابل للذوبان في المذيبات العضوية مثل الكحول والإيثرات والكلوروفورم |
| ضغط البخار | 10.7 ملم زئبق عند 20 درجة مئوية |
| كثافة بخار | 3.7 |
| pKa | 10.17 |
| الرقم الهيدروجيني | غير قابل للتطبيق |
سلامة ومخاطر إيثيل بنزين
يمكن أن يكون C8H10 خطيرًا إذا لم يتم اتخاذ الاحتياطات المناسبة عند التعامل معه واستخدامه. ويصنف على أنه سائل قابل للاشتعال وقد يشتعل إذا تعرض للحرارة أو اللهب. يمكن أن يكون C8H10 ضارًا أيضًا في حالة استنشاقه أو ابتلاعه. التعرض لتركيزات عالية من C8H10 قد يسبب الدوخة والصداع وتهيج الجهاز التنفسي. ارتبط التعرض طويل الأمد لـ C8H10 بتلف الكبد والكلى. يجب اتخاذ احتياطات السلامة عند العمل مع C8H10، مثل ارتداء ملابس وقفازات واقية، والعمل في مناطق جيدة التهوية، وتخزينها في مكان آمن وبارد وجاف.
| رموز الخطر | قابلة للاشتعال، ضارة |
| وصف الأمان | الابتعاد عن الحرارة والشرر واللهب المكشوف والأسطح الساخنة. استخدم معدات مقاومة للانفجار. تجنب استنشاق الغبار/الأبخرة/الغاز/الضباب/الأبخرة/الرذاذ. يغسل جيدا بعد المناولة. |
| أرقام تعريف الأمم المتحدة | رقم الأمم المتحدة 1175 |
| رمز النظام المنسق | 2902.90.20 |
| فئة الخطر | 3 (السوائل القابلة للاشتعال) |
| مجموعة التعبئة | الثاني (خطر متوسط) |
| تسمم | يعتبر إيثيل بنزين مادة سامة إلى حد ما. يمكن أن يسبب تهيج العين والجلد، ومشاكل في الجهاز التنفسي وتلف الجهاز العصبي إذا كان التعرض لفترة طويلة أو بتركيزات عالية. |
طرق تخليق إيثيل بنزين
الطريقة الأكثر استخدامًا لتصنيع C8H10 هي إزالة الهيدروجين الحفزي لإيثيل سيكلوهكسان. تتضمن هذه العملية تسخين خليط من إيثيل سيكلوهكسان وغاز الهيدروجين فوق محفز عند درجة حرارة عالية، مما يؤدي إلى انفصال ذرات الهيدروجين عن مجموعة الإيثيل، مما يؤدي إلى تكوين C8H10.
هناك طريقة أخرى لتصنيع C8H10 تتضمن ألكلة البنزين مع غاز الإيثيلين . يتطلب هذا التفاعل محفزًا، عادةً كلوريد الألومنيوم، وينتج عنه تكوين C8H10 وكلوريد الهيدروجين كمنتج ثانوي.
تتضمن الطريقة البديلة لإنتاج C8H10 تفاعل البنزين مع كلوريد الإيثيل في وجود محفز حمض لويس، مثل كلوريد الألومنيوم. تؤدي هذه العملية إلى تكوين C8H10 وكلوريد الهيدروجين كمنتج ثانوي.
إلى جانب الطرق المذكورة، يقوم الباحثون أيضًا بتطوير طرق جديدة لتصنيع C8H10، مثل استخدام السوائل الأيونية كمذيب لألكلة الإيثيلين للبنزين . هذه الأساليب لديها القدرة على تقديم فوائد من حيث الكفاءة والاستدامة البيئية. ومع ذلك، فإن استخدامها الصناعي لم ينتشر بعد على نطاق واسع.
استخدامات إيثيل بنزين
لدى C8H10 العديد من الاستخدامات المهمة في مختلف الصناعات. بعض استخداماته الرئيسية هي:
- إنتاج الستايرين: إنتاج الستايرين، الذي يستخدم في صناعة مجموعة متنوعة من المواد البلاستيكية والراتنجات والمطاط الصناعي، المرتبط بـ C8H10 كوسيط رئيسي.
- المذيب: يستخدم عادة كمذيب لمختلف التطبيقات، بما في ذلك الأحبار والطلاء والمواد اللاصقة ومنتجات التنظيف.
- مادة مضافة للوقود: تضاف إلى البنزين لتحسين نسبة الأوكتان فيه، مما يؤدي إلى تحسين أداء المحرك.
- الوسيط الكيميائي: يستخدم كمادة خام لتخليق مواد كيميائية أخرى، مثل الفينيل إيثانول وثنائي إيثيل بنزين.
- إنتاج البوليمرات: يستخدم في إنتاج أنواع مختلفة من البوليمرات، مثل راتنجات البوليسترين والأكريلونتريل بوتادين ستايرين (ABS).
- الزراعة: يستخدم أيضًا كمبيد للآفات ومبيدات الأعشاب.
- التطبيقات الطبية: يستخدم كمخدر موضعي، وكذلك كمذيب للمنتجات الصيدلانية.
أسئلة:
س: كم عدد الإشارات التي تتوقع رؤيتها في طيف الرنين المغناطيسي النووي 1H للإيثيل بنزين؟
ج: طيف الرنين المغناطيسي النووي 1H لـ C8H10 سيكون له أربع إشارات: اثنتان للبروتونات الموجودة على حلقة البنزين (والتي قد تظهر على شكل ثنائي) واثنتان للبروتونات الموجودة على مجموعة الإيثيل (والتي قد تظهر على شكل ثلاثية).
س: ما هي نسب البنزين والإيثيل بنزين التي يجب خلطها؟
ج: تعتمد نسب البنزين وC8H10 المراد خلطها على التركيز المطلوب لـC8H10 في الخليط. يمكن أن تختلف نسبة البنزين/C8H10 من 10:1 إلى 1:1، حسب التطبيق.
س: ما هي نترات إيثيل بنزين؟
ج: تشتمل نترجة C8H10 على تفاعل C8H10 مع خليط من حمض النيتريك وحمض الكبريتيك، مما يؤدي إلى إدخال واحدة أو أكثر من مجموعات النيترو في حلقة البنزين في C8H10. يستخدم هذا التفاعل بشكل شائع في إنتاج المواد الكيميائية الصناعية مثل النيتروبنزين والفينيل إيثيلامين.
س: هل إيثيل بنزين قطبي؟
ج: C8H10 مركب غير قطبي بسبب البنية المتماثلة لحلقة البنزين، مما ينفي أي قطبية لمجموعة الإيثيل. ونتيجة لذلك، فإن C8H10 لديه قابلية منخفضة للذوبان في الماء وقابل للذوبان بشكل عام في المذيبات غير القطبية مثل الهكسان والتولوين.
س: كيف يتم التغيير من إيثيل بنزين إلى ستايرين؟
ج: يمكن تحويل C8H10 إلى ستيرين من خلال عملية نزع الهيدروجين، والتي تتضمن إزالة ذرتي هيدروجين من مجموعة الإيثيل باستخدام محفز مثل أكسيد الحديد أو أكسيد الكروم. تؤدي هذه العملية إلى تكوين غاز الستايرين والهيدروجين كمنتج ثانوي. يمكن بعد ذلك تنقية الستايرين الناتج واستخدامه في إنتاج مواد صناعية مختلفة مثل البلاستيك والراتنجات والمطاط الصناعي.
