أميد الصوديوم (NaNH2) مركب كيميائي. وهي مكونة من ذرات الصوديوم والنيتروجين. يتم استخدامه كقاعدة قوية في التفاعلات الكيميائية المختلفة.
| اسم الأيوباك | أميد الصوديوم |
| الصيغة الجزيئية | هيدروكسيد الصوديوم2 |
| CAS رقم | 7782-92-5 |
| المرادفات | سوداميد، أزانيد الصوديوم، أميد الصوديوم، نيتريد الصوديوم |
| إنتشي | إنشي = 1S/NaN2/c2-1-3/q-1 |
خصائص أميد الصوديوم
صيغة أميد الصوديوم
صيغة أميد الصوديوم هي NaNH2. وتتكون من ذرة صوديوم (Na) وذرة هيدروجين (H) وذرة نيتروجين (N). تمثل هذه الصيغة الكيميائية تركيبة أميد الصوديوم على المستوى الجزيئي.
أميد الصوديوم الكتلة المولية
يتم حساب الكتلة المولية لأزانيد الصوديوم عن طريق إضافة الكتل الذرية للعناصر المكونة له. تبلغ الكتلة الذرية للصوديوم 22.99 جرامًا لكل مول (جم / مول) والكتلة الذرية للنيتروجين 14.01 جم / مول. وبإضافة هذه القيم، نرى أن الكتلة المولية لأزانيد الصوديوم تبلغ حوالي 39 جم/مول.
نقطة غليان أميد الصوديوم
نقطة غليان أزانيد الصوديوم هي درجة الحرارة التي يتحول عندها من سائل إلى غاز. أزانيد الصوديوم لديه نقطة غليان عالية نسبيًا تبلغ حوالي 850 درجة مئوية (درجة مئوية). عند درجة الحرارة هذه، يتم التغلب على القوى الجزيئية التي تربط جزيئات أزانيد الصوديوم معًا، مما يؤدي إلى التحول من الحالة السائلة إلى الحالة الغازية.
أميد الصوديوم نقطة الانصهار
نقطة انصهار أزانيد الصوديوم هي درجة الحرارة التي يتحول عندها من مادة صلبة إلى سائلة. أزانيد الصوديوم لديه نقطة انصهار منخفضة نسبيًا تبلغ حوالي 210 درجة مئوية (درجة مئوية). عند درجة الحرارة هذه، ينهار هيكل الشبكة البلورية لأزانيد الصوديوم الصلب، مما يسمح للجزيئات بالتحرك بحرية، وتشكيل سائل.
كثافة أميد الصوديوم جم/مل
كثافة أزانيد الصوديوم هي مقياس لكتلته لكل وحدة حجم. تبلغ كثافة أزانيد الصوديوم حوالي 1.39 جرام لكل مليلتر (جم / مل). تشير هذه القيمة إلى أن أزانيد الصوديوم مادة كثيفة نسبيًا.
أميد الصوديوم الوزن الجزيئي
الوزن الجزيئي لأزانيد الصوديوم هو مجموع الأوزان الذرية لجميع الذرات الموجودة في صيغته الكيميائية. يبلغ الوزن الجزيئي لأزانيد الصوديوم حوالي 39 جرامًا لكل مول (جم / مول).
هيكل أميد الصوديوم
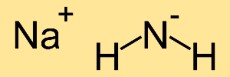
يتكون هيكل أزانيد الصوديوم من ذرة صوديوم واحدة (Na) مرتبطة بذرتين من النيتروجين (N). تشكل ذرات النيتروجين ترتيبًا خطيًا مع ذرة الصوديوم في المنتصف، مما ينتج عنه بنية جزيئية خطية.
ذوبان أميد الصوديوم
أزانيد الصوديوم ضعيف الذوبان في الماء. يتفاعل مع الماء لتكوين هيدروكسيد الصوديوم (NaOH) والأمونيا (NH3). ومع ذلك، فهو قابل للذوبان في بعض المذيبات العضوية مثل الأمونيا السائلة والكحوليات السائلة. إن قابلية ذوبان أزانيد الصوديوم في هذه المذيبات تسمح باستخدامه في التفاعلات الكيميائية المختلفة.
| مظهر | الصلبة البيضاء |
| جاذبية معينة | 1.39 جرام/مل |
| لون | أبيض |
| يشم | تشبه الأمونيا |
| الكتلة المولية | 39 جرام/مول |
| كثافة | 1.39 جرام/مل |
| نقطة الانصهار | 210 درجة مئوية |
| نقطة الغليان | 850 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | يتفاعل |
| الذوبان | قابل للذوبان في المذيبات العضوية مثل الأمونيا السائلة والكحوليات السائلة |
| ضغط البخار | غير قابل للتطبيق |
| كثافة بخار | غير قابل للتطبيق |
| pKa | غير قابل للتطبيق |
| الرقم الهيدروجيني | القلوية (فوق 7) |
سلامة ومخاطر أميد الصوديوم
يشكل أزانيد الصوديوم بعض مخاطر السلامة والمخاطر التي يجب أخذها في الاعتبار. يتفاعل بعنف مع الماء، ويطلق غاز الأمونيا السام وهيدروكسيد الصوديوم المسبب للتآكل. ولذلك يجب التعامل معه بحذر شديد لتجنب ملامسته للرطوبة أو الماء. أزانيد الصوديوم هو أيضًا قاعدة قوية يمكن أن تسبب حروقًا شديدة وتلفًا للعين إذا لامست الجلد أو العينين. استنشاق غباره أو أبخرةه قد يهيج الجهاز التنفسي. ومن المستحسن ارتداء معدات الحماية المناسبة، مثل القفازات والنظارات الواقية وجهاز التنفس الصناعي، عند العمل مع أزانيد الصوديوم. تعتبر التهوية والتخزين المناسبين بعيدًا عن المواد غير المتوافقة من تدابير السلامة الأساسية.
| رموز الخطر | أكالة، ضارة، سامة |
| وصف الأمان | تعامل بحذر شديد. تجنب ملامسة الماء/الرطوبة. ارتداء معدات الحماية. مطلوب التهوية والتخزين الكافية. |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 1410 |
| رمز النظام المنسق | 28500020 |
| فئة الخطر | 4.3 (خطر عندما يكون مبللاً)، 6.1 (سام)، 8 (مسبب للتآكل) |
| مجموعة التعبئة | ثانيا |
| تسمم | سامة عن طريق الابتلاع أو الاستنشاق أو ملامسة الجلد/العين |
طرق تصنيع أميد الصوديوم
هناك طرق مختلفة لتجميع أزانيد الصوديوم.
الطريقة الشائعة هي التفاعل بين الصوديوم المعدني والأمونيا الغازية (NH3) . في هذه العملية، يتفاعل معدن الصوديوم مع غاز الأمونيا تحت ظروف خاضعة للرقابة لإنتاج أزانيد الصوديوم. ويحدث التفاعل عادة في وعاء مفاعل مجهز بتدابير السلامة المناسبة.
تتضمن الطريقة الأخرى التفاعل بين هيدريد الصوديوم (NaH) وغاز الأمونيا . يتفاعل هيدريد الصوديوم، وهو مركب صلب، مع غاز الأمونيا لإنتاج أزانيد الصوديوم وغاز الهيدروجين. غالبًا ما تستخدم الأجواء الخاملة لتنفيذ هذا التفاعل لتجنب التفاعلات الجانبية غير المرغوب فيها.
بالإضافة إلى ذلك، فإن التفاعل بين الصوديوم المعدني والأمونيا السائلة يسمح بتحضير أزانيد الصوديوم. تتضمن هذه الطريقة إذابة معدن الصوديوم في الأمونيا السائلة، مما يؤدي إلى تكوين أزانيد الصوديوم وغاز الهيدروجين.
لتصنيع أزانيد الصوديوم، يتفاعل أزيد الصوديوم (NaN3) مع هيدروكسيد الصوديوم (NaOH). التفاعل بين هذين المركبين ينتج أزانيد الصوديوم بالإضافة إلى إطلاق غاز النيتروجين.
تجدر الإشارة إلى أن هذه الطرق الاصطناعية تتطلب الخبرة واحتياطات السلامة المناسبة بسبب التفاعل والمخاطر المرتبطة بأزانيد الصوديوم.
استخدامات أميد الصوديوم
يجد أزانيد الصوديوم تطبيقات في مختلف المجالات بسبب خصائصه الفريدة. وهذه بعض استخداماته:
- قاعدة قوية في تفاعلات الكيمياء العضوية: يقوم أزانيد الصوديوم بإزالة البروتونات من الأحماض الضعيفة، مما يسهل تخليق المركبات العضوية المختلفة.
- مصدر النيتروجين في التفاعلات: يدخل أزانيد الصوديوم ذرات النيتروجين في الجزيئات العضوية، ويلعب دورًا حاسمًا في تركيب المستحضرات الصيدلانية والأصباغ والبوليمرات.
- نزع الهلجنة الهيدروجينية: يزيل أزانيد الصوديوم هاليدات الهيدروجين من المركبات العضوية في تفاعلات إزالة الهلجنة الهيدروجينية. تسهل هذه العملية تحضير الألكينات والألكاينات والمركبات الأخرى غير المشبعة.
- تفاعلات فتح الحلقة: يشارك أزانيد الصوديوم في تفاعلات فتح الحلقة للمركبات الحلقية، مثل تخليق غابرييل، وتحويل الأمينات الحلقية إلى أمينات أولية.
- إزالة الكبريت: يمكن لأزانيد الصوديوم إزالة ذرات الكبريت من المركبات العضوية، مما يتيح تفاعلات إزالة الكبريت. وهذا مفيد في إنتاج الوقود الخالي من الكبريت وفي تقليل التأثير البيئي للمركبات المحتوية على الكبريت.
- تخزين الهيدروجين: درس الباحثون الاستخدام المحتمل لأزانيد الصوديوم في أنظمة تخزين الهيدروجين. يمكن أن يتفاعل مع غاز الهيدروجين، مكونًا هيدريد الصوديوم، والذي يمكنه بعد ذلك إطلاق الهيدروجين عند التسخين.
- دعم المحفز: يمكن أن يعمل أزانيد الصوديوم كمحفز، مما يحسن أداء بعض التفاعلات التحفيزية. فهو يضمن الاستقرار ويحسن كفاءة المواد الحفازة في التحولات الكيميائية المختلفة.
بشكل عام، خصائص أزانيد الصوديوم المتنوعة تجعله مركبًا قيمًا في التخليق العضوي، وكيمياء النيتروجين، والتطبيقات الصناعية الأخرى.
أسئلة:
س: ماذا يفعل NaNH2؟
ج: NaNH2 عبارة عن قاعدة قوية شائعة الاستخدام في تفاعلات الكيمياء العضوية لإزالة بروتونات الأحماض الضعيفة وتسهيل التحولات المختلفة.
س: ما هو NaNH2؟
ج: NaNH2 هو أميد الصوديوم، وهو مركب كيميائي يتكون من أيونات الصوديوم (Na) والأزانيد (NH2)، وغالبًا ما يستخدم ككاشف وقاعدة قوية في التخليق العضوي.
س: ما هو استخدام NaNH2 المفرط؟
ج: يمكن أن يؤدي فائض NaNH2 إلى إزالة بروتونات إضافية لذرات الهيدروجين الحمضية في التفاعل، وبالتالي زيادة مدى نزع البروتونات وربما تغيير نتيجة التفاعل.
س: ماذا يفعل NaNH2 للألكين؟
ج: يمكن لـ NaNH2 استخلاص ذرة هيدروجين من الألكين، مما يؤدي إلى تكوين ألكان ومركب ألكوكسيد الصوديوم.
س: ماذا يفعل NaNH2 للبروموبنزين؟
ج: يمكن أن يحل NaNH2 محل ذرة البروم في البروموبنزين من خلال تفاعل الاستبدال المحب للنواة، مما يؤدي إلى تكوين فينيل أمين الصوديوم.
س: هل NaNH2 قاعدة قوية؟
ج: نعم، NaNH2 عبارة عن قاعدة قوية قادرة على قبول البروتونات ونزع بروتونات الأحماض الضعيفة بسبب وجود أيون الأميد.
س: ما التفاعل الذي يحدث إذا أضيف H2O إلى خليط NaNH2/NH3؟
ج: إن إضافة H2O إلى خليط NaNH2/NH3 يؤدي إلى توليد غاز الأمونيا (NH3) وهيدروكسيد الصوديوم (NaOH) بسبب التفاعل بين الماء والقاعدة القوية NaNH2.
س: ما الوسيط الذي يدخل في هذا التفاعل: NaNH2 + NH3 السائل؟
ج: الوسيط المستخدم في تفاعل NaNH2 مع NH3 السائل هو إلكترون مذاب، يتكون من منح إلكترون من الصوديوم إلى الأمونيا.
س: هل NaNH2 محب للنواة بشكل جيد؟
ج: نعم، يمكن أن يعمل NaNH2 باعتباره محبًا جيدًا للنواة نظرًا لقدرته على التبرع بزوج من الإلكترونات والمشاركة في تفاعلات الاستبدال النيوكليوفيلية.
س: هل NaNH2 أيوني أم تساهمي؟
ج: NaNH2 مركب أيوني يتكون من أيونات الصوديوم الموجبة (Na+) وأيونات الأميد سالبة الشحنة (NH2-).
س: هل يتفاعل 2-هيكسين مع أميد الصوديوم؟
ج: نعم، يمكن أن يتفاعل 2-هيكسين مع أميد الصوديوم، مما يؤدي إلى تكوين أسيتيليد الصوديوم ومركب الألكاين المقابل.
س: ما هي أقوى قاعدة بين أميد الصوديوم وفينوكسات الصوديوم؟
ج: أزانيد الصوديوم هو القاعدة الأقوى من فينوكسات الصوديوم بسبب قاعدية أيون الأميد (NH2-) الأكبر مقارنة بأيون الفينوكس (C6H5O-).
