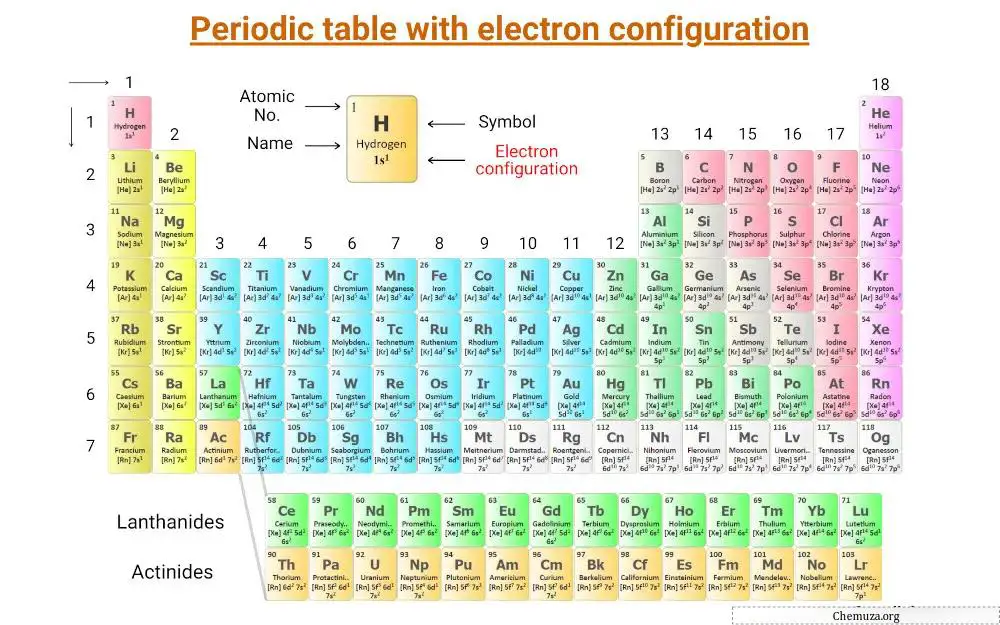
وهو جدول دوري يُشار إليه بالترتيب الإلكتروني للعناصر.
يمكنك أيضًا تنزيل صورة عالية الدقة من هنا؛
دعونا نستكشف التكوينات الإلكترونية للعناصر بشكل أكبر؛
ما هو التكوين الإلكتروني؟
يشير التكوين الإلكتروني إلى ترتيب الإلكترونات في الذرة .
الإلكترونات هي جسيمات صغيرة ذات شحنة سالبة تدور حول نواة الذرة ذات الشحنة الموجبة .
يحدد التكوين الإلكتروني للذرة خصائصها الكيميائية والفيزيائية، مثل تفاعلها، وموصليتها، ونقطة الانصهار.
يتم تحديد ترتيب الإلكترونات في الذرة من خلال مستويات الطاقة (وتسمى أيضًا الأغلفة) والمجالات الفرعية المحددة داخل تلك الأغلفة.
عادةً ما يتم تمثيل التكوين الإلكتروني باستخدام علامة تشير إلى عدد الإلكترونات في كل غلاف ومدار فرعي، ويتبع قواعد معينة بناءً على مبادئ ميكانيكا الكم.
ما هي الأصداف (n) والأصداف الفرعية (s، p، d، f)؟
الغلاف: الغلاف هو المدار الذي تدور فيه الإلكترونات حول نواة الذرة.
يتم تعيين رقم (n) لكل غلاف، بدءًا من رقم للغلاف الأول ويزداد مع كل غلاف إضافي.
يمكن للغلاف الأول أن يحتوي على إلكترونين فقط كحد أقصى، بينما يمكن للغلاف الثاني أن يحمل ما يصل إلى 8 إلكترونات، ويمكن للأغلفة اللاحقة أن تحتوي على أكثر من ذلك.
الغلاف الفرعي (أو المدارات): يوجد داخل كل غلاف مدارات فرعية مختلفة، والتي يتم تمييزها باستخدام حروف مثل s وp وd وf.
يمكن أن يحتوي المستوى الفرعي s على 2 إلكترون كحد أقصى، ويمكن أن يحتوي المستوى الفرعي p على ما يصل إلى 6 إلكترونات، ويمكن أن يحتوي المستوى الفرعي d على ما يصل إلى 10 إلكترونات، ويمكن أن يحتوي المستوى الفرعي f على ما يصل إلى 14 إلكترونًا. [1]
تحدد طبقات الذرة وطبقاتها الفرعية تكوينها الإلكتروني، والذي بدوره يحدد خصائصها الكيميائية والفيزيائية.
التكوين الإلكتروني للعناصر (قائمة)
فيما يلي قائمة بالتكوينات الإلكترونية للعناصر العشرين الأولى في الجدول الدوري.
| العدد الذري | عنصر | التكوين الإلكترونية |
| 1 | الهيدروجين (ح) | 1س 1 |
| 2 | هيليوم (هو) | 1س 2 |
| 3 | الليثيوم (لي) | [هو] 2س 1 |
| 4 | البريليوم (كن) | [هو] 2س 2 |
| 5 | البورون (ب) | [هو] 2ق 2 2ف 1 |
| 6 | الكربون (ج) | [هو] 2س 22 ف 2 |
| 7 | النيتروجين (ن) | [هو] 2س 22 ف 3 |
| 8 | الأكسجين (س) | [هو] 2س 22 ف 4 |
| 9 | فلوريت (F) | [هو] 2ق 22 ف 5 |
| عشرة | نيون (ني) | [هو] 2س 22 ف 6 |
| 11 | الصوديوم (نا) | [فعل] 3س 1 |
| 12 | المغنيسيوم (ملغ) | [افعل] 3ث 2 |
| 13 | الألومنيوم (آل) | [فعل] 3س 2 3ع 1 |
| 14 | السيليكون (سي) | [لا] 3س 2 3ف 2 |
| 15 | الفوسفور (ف) | [لا] 3س 2 3ف 3 |
| 16 | الكبريت (S) | [فعل] 3س 2 3ف 4 |
| 17 | الكلور (الكلور) | [لا] 3س 2 3ف 5 |
| 18 | الأرجون (آر) | [فعل] 3س 2 3ف 6 |
| 19 | البوتاسيوم (ك) | [ع] 4س 1 |
| 20 | الكالسيوم (كاليفورنيا) | [ع] 4س 2 |
