NH4OH أو هيدروكسيد الأمونيوم هو محلول واضح عديم اللون يعرف عادة باسم الأمونيا المنزلية. وهو محلول قلوي بقوة مع درجة حموضة 11-12. يتم استخدامه كعامل تنظيف، وفي إنتاج الأسمدة وفي بعض التطبيقات الغذائية كعامل ترك.
| اسم الأيوباك | هيدروكسيد الأمونيوم |
| الصيغة الجزيئية | NH4OH |
| CAS رقم | 1336-21-6 |
| المرادفات | محلول الأمونيا، الأمونيا المائية، الأمونيا المنزلية |
| إنتشي | InChI=1S/H5NO/c1-5(2,3)4/h(H,1,2,3,4)/p+1 |
خصائص هيدروكسيد الأمونيوم
صيغة هيدروكسيد الأمونيوم
الصيغة الكيميائية لهيدروكسيد الأمونيوم هي NH4OH. تمثل الصيغة العدد النسبي للذرات وأنواعها في المركب. يمثل “N” النيتروجين، و”H” يمثل الهيدروجين، و”O” يمثل الأكسجين. تشير الأرقام الفهرسية في الصيغة إلى عدد ذرات كل عنصر في المركب. في حالة هيدروكسيد الأمونيوم، هناك ذرة نيتروجين واحدة وأربع ذرات هيدروجين وذرة أكسجين واحدة. تمثل صيغة هيدروكسيد الأمونيوم المركب الأيوني، الذي يتكون من أيونات الأمونيوم موجبة الشحنة (NH4+) وأيونات هيدروكسيد سالبة الشحنة (OH-).
هيدروكسيد الأمونيوم ف
الرقم الهيدروجيني لهيدروكسيد الأمونيوم (NH4OH) أساسي، حيث تبلغ قيمته حوالي 11. وهذا يعني أن هيدروكسيد الأمونيوم يحتوي على تركيز عالٍ من أيونات الهيدروكسيد (OH-) وهو قلوي جدًا. يمكن أن يختلف الرقم الهيدروجيني لمحاليل هيدروكسيد الأمونيوم اعتمادًا على التركيز ودرجة الحرارة وعوامل أخرى، ولكنه يعتبر عمومًا قاعدة قوية ذات درجة حموضة أعلى من 7.0. يستخدم هيدروكسيد الأمونيوم بشكل شائع في العديد من التطبيقات الصناعية والمنزلية، مثل التنظيف وتعديل درجة الحموضة، بسبب قلويته العالية. ومع ذلك، من المهم التعامل مع هيدروكسيد الأمونيوم بحذر، لأنه يمكن أن يكون مسببًا للتآكل وخطيرًا إذا لم يتم التعامل معه بشكل صحيح.
هيدروكسيد الأمونيوم SDS
يرمز MSDS إلى ورقة بيانات سلامة المواد، وهي وثيقة توفر معلومات حول خصائص المادة الكيميائية ومعالجتها وتخزينها والتخلص منها. ستوفر صحيفة بيانات سلامة المواد (MSDS) الخاصة بهيدروكسيد الأمونيوم (NH4OH) معلومات عن خصائصه الفيزيائية والكيميائية، والآثار الصحية المحتملة، ومخاطر الحرائق والانفجارات، وأي تدابير وقائية ينبغي اتخاذها عند التعامل مع المادة أو استخدامها.
ستتضمن صحيفة بيانات سلامة المواد (MSDS) الخاصة بهيدروكسيد الأمونيوم أيضًا معلومات عن سميته وتفاعله وقابليته للاشتعال، بالإضافة إلى أي تدابير إسعافات أولية مناسبة في حالة التعرض. بالإضافة إلى ذلك، ستوفر صحيفة بيانات سلامة المواد معلومات حول التخزين والتخلص المناسبين من هيدروكسيد الأمونيوم، بما في ذلك أي احتياطات ضرورية لمنع الانسكابات أو التسربات.
ذوبان هيدروكسيد الأمونيوم
هيدروكسيد الأمونيوم (NH4OH) شديد الذوبان في الماء. وهو يشكل محلولًا شفافًا عديم اللون وشديد القلوية وله رائحة مميزة. تعتمد ذوبان هيدروكسيد الأمونيوم في الماء على درجة الحرارة والتركيز، مع ارتفاع درجات الحرارة والتركيزات مما يؤدي إلى زيادة الذوبان.
بشكل عام، يذوب هيدروكسيد الأمونيوم بسهولة في الماء، مما ينتج محلولًا محايدًا إلى قلويًا بدرجة حموضة تتراوح من 9 إلى 11 تقريبًا. وتتأثر قابلية ذوبان هيدروكسيد الأمونيوم في الماء أيضًا بعوامل أخرى مثل الضغط ودرجة الحرارة ووجود عوامل أخرى. المواد الذائبة.
هيدروكسيد الأمونيوم الكتلة المولية
الكتلة المولية لهيدروكسيد الأمونيوم (NH4OH) هي 35.05 جم/مول. هذه القيمة مهمة لتحديد كمية هيدروكسيد الأمونيوم في العينة، وكذلك للتفاعلات الكيميائية التي تنطوي على المركب. لتحديد الكتلة المولية لمادة ما، يتم جمع الأوزان الذرية لجميع العناصر الموجودة في المركب معًا. في حالة هيدروكسيد الأمونيوم، يتم حساب الكتلة المولية عن طريق إضافة الأوزان الذرية للنيتروجين (14.01 جم / مول)، الهيدروجين (1.01 جم / مول) والأكسجين (16.00 جم / مول).
نقطة غليان هيدروكسيد الأمونيوم
تبلغ درجة غليان هيدروكسيد الأمونيوم حوالي 38 درجة مئوية. وهذه القيمة مهمة في تحديد الظروف التي في ظلها يتحول المركب من سائل إلى غاز. أوجد درجة غليان هيدروكسيد الأمونيوم عن طريق قياس ضغط بخار المادة. ضغط البخار هو الضغط الذي يمارسه البخار فوق السائل الموجود في حاوية مغلقة. ضع في اعتبارك أن نقطة الغليان يمكن أن تتغير أيضًا اعتمادًا على الضغط ودرجة الحرارة.
نقطة انصهار هيدروكسيد الأمونيوم
نقطة انصهار هيدروكسيد الأمونيوم هي -77 درجة مئوية. هذه القيمة مهمة في تحديد الظروف التي يتغير فيها المركب من الحالة الصلبة إلى الحالة السائلة. قم بقياس نقطة انصهار هيدروكسيد الأمونيوم من خلال تقييم قوة روابطه بين الجزيئات. تذكر أن نقطة الانصهار يمكن أن تختلف تبعًا لضغط ودرجة حرارة البيئة المحيطة.
كثافة هيدروكسيد الأمونيوم جم/مل
تبلغ كثافة هيدروكسيد الأمونيوم حوالي 0.91 جم / مل. هذه القيمة مهمة لتحديد كمية هيدروكسيد الأمونيوم في حجم معين، وكذلك لحساب كتلة المادة في حجم معين. تحديد كثافة هيدروكسيد الأمونيوم عن طريق قسمة كتلته على الحجم الذي يشغله. ضع في اعتبارك أن كثافة المادة يمكن أن تتغير اعتمادًا على درجة الحرارة والضغط.
الوزن الجزيئي لهيدروكسيد الأمونيوم
الوزن الجزيئي لهيدروكسيد الأمونيوم هو 35.05 جم / مول. هذه القيمة مهمة لتحديد كمية هيدروكسيد الأمونيوم في العينة، وكذلك للتفاعلات الكيميائية التي تنطوي على المركب. حساب الوزن الجزيئي لهيدروكسيد الأمونيوم عن طريق إضافة الأوزان الذرية للنيتروجين (14.01 جم/مول)، الهيدروجين (1.01 جم/مول)، والأكسجين (16.00 جم/مول).
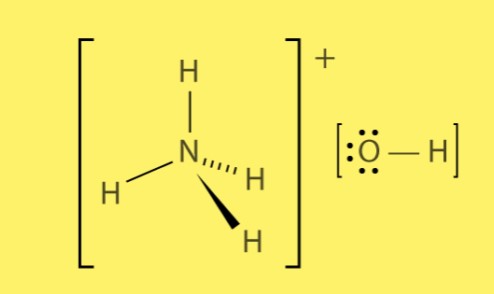
هيكل هيدروكسيد الأمونيوم
يتكون هيدروكسيد الأمونيوم من مزيج أيونات الأمونيوم موجبة الشحنة (NH4+) وأيونات هيدروكسيد سالبة الشحنة (OH-). الروابط الأيونية بين هذه الأيونات تخلق جاذبية كهروستاتيكية قوية، مما يؤدي إلى تكوين المركب.
| مظهر | سائل واضح عديم اللون |
| جاذبية معينة | 0.91 جرام/مل |
| لون | عديم اللون |
| يشم | رائحة نفاذة تشبه الأمونيا |
| الكتلة المولية | 35.05 جم/مول |
| كثافة | 0.91 جرام/مل |
| نقطة الانصهار | -77 درجة مئوية |
| نقطة الغليان | 38 درجة مئوية |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | قابل للذوبان تماما |
| الذوبان | قابل للذوبان في الإيثانول والميثانول |
| ضغط البخار | 17.5 ملم زئبق عند 20 درجة مئوية |
| كثافة بخار | 0.6 (الهواء = 1) |
| pKa | 10.64 |
| الرقم الهيدروجيني | 11.6 (حل 1M) |
سلامة ومخاطر هيدروكسيد الأمونيوم
هيدروكسيد الأمونيوم هو محلول قلوي قوي ويمكن أن يكون خطيرًا إذا تم التعامل معه بشكل خاطئ. قد يسبب تهيج الجلد والعين ومشاكل في الجهاز التنفسي إذا تم استنشاقه. في حالة ملامسة الجلد، يجب شرب الكثير من الماء واستشارة الطبيب إذا لزم الأمر. إذا ابتلع، فإنه يمكن أن يسبب ضررا خطيرا أو الموت. ولذلك فمن المهم أن يبقيه بعيدا عن متناول الأطفال والحيوانات الأليفة. كما أنه قابل للاشتعال ويجب إبعاده عن مصادر الحرارة واللهب. عند استخدام هيدروكسيد الأمونيوم، من المهم ارتداء معدات الحماية مثل القفازات وحماية العين. في حالة الانسكاب، قم بمعادلته بالحمض ونظفه بتهوية كافية. تعتبر مراقبة احتياطات السلامة والتخزين المناسب ضرورية عند التعامل مع هيدروكسيد الأمونيوم.
| رموز الخطر | تآكل |
| وصف الأمان | س26، س37/39 |
| أرقام تعريف الأمم المتحدة | UN2672 |
| رمز النظام المنسق | 2814.10.00 |
| فئة الخطر | 8 |
| مجموعة التعبئة | ثانيا |
| تسمم | ضار إذا تم ابتلاعه أو استنشاقه أو ملامسته للجلد. قد يسبب تهيجًا وحروقًا شديدة. |
طرق تصنيع هيدروكسيد الأمونيوم
يمكن تصنيع هيدروكسيد الأمونيوم بطريقتين رئيسيتين: عملية كلوريد الأمونيوم وعملية الأمونيا.
تتضمن عملية كلوريد الأمونيوم تفاعل غاز الأمونيا وحمض الهيدروكلوريك لإنتاج كلوريد الأمونيوم والماء:
NH3 + حمض الهيدروكلوريك → NH4Cl + H2O
ثم يتم إذابة كلوريد الأمونيوم في الماء لإنتاج محلول هيدروكسيد الأمونيوم. يمكن زيادة تركيز هذا المحلول بالتقطير لإنتاج محلول مركز من هيدروكسيد الأمونيوم.
تتضمن عملية الأمونيا التفاعل المباشر لغاز الأمونيا والماء، لإنتاج هيدروكسيد الأمونيوم وغاز الهيدروجين:
NH3 + H2O → NH4OH + H2
يمكن التحكم في إنتاج هيدروكسيد الأمونيوم عن طريق ضبط درجة الحرارة والضغط أثناء التفاعل الطارد للحرارة، مما يؤدي إلى الحصول على محلول يمكن تنقيته وتركيزه من خلال تقنيات الغسيل والتقطير. يستخدم الإنتاج الصناعي لهيدروكسيد الأمونيوم عادة عملية الأمونيا بسبب بساطتها وكفاءتها، ولكن عملية كلوريد الأمونيوم تعمل كخيار احتياطي أثناء نقص الأمونيا.
استخدامات هيدروكسيد الأمونيوم
لهيدروكسيد الأمونيوم استخدامات عديدة في صناعات مختلفة. بعض تطبيقاته الشائعة هي:
- في مختلف التطبيقات المنزلية والصناعية، يتم استخدام هيدروكسيد الأمونيوم كعامل تنظيف لإزالة الشحوم والزيوت والأوساخ بشكل فعال من الأسطح.
- وفي صناعة المواد الغذائية، يتم استخدامه كمطهر لقتل البكتيريا ومسببات الأمراض على الأسطح الملامسة للأغذية. في الزراعة، يوفر هيدروكسيد الأمونيوم النيتروجين الأساسي كسماد لنمو النبات وهو عنصر رئيسي في إنتاج سماد نترات الأمونيوم.
- وفي صناعة الأدوية، يتم استخدامه في إنتاج بعض الأدوية وكمنظم للأس الهيدروجيني في تصنيع بعض المنتجات الطبية.
- تستخدم صناعة الخبز هيدروكسيد الأمونيوم كعامل ترك لجعل العجين يرتفع، ويعمل أيضًا كعامل نكهة في بعض المنتجات الغذائية وكمنظم للأس الهيدروجيني في إنتاج بعض الأطعمة والمشروبات.
- في صناعة النسيج، يعمل هيدروكسيد الأمونيوم على تحييد الأحماض وضبط مستويات الرقم الهيدروجيني في إنتاج المنسوجات. وفي معالجة المياه، يقوم بضبط مستويات الرقم الهيدروجيني وإزالة الشوائب.
بشكل عام، يعتبر هيدروكسيد الأمونيوم مادة كيميائية متعددة الاستخدامات وتستخدم على نطاق واسع، ولها تطبيقات في مختلف الصناعات. ومع ذلك، من المهم التعامل مع هيدروكسيد الأمونيوم بأمان، لأنه قد يكون خطيرًا إذا لم يتم التعامل معه بشكل صحيح.
أسئلة:
هل هيدروكسيد الأمونيوم قابل للذوبان؟
نعم، هيدروكسيد الأمونيوم شديد الذوبان في الماء. وهو يشكل محلولًا شفافًا عديم اللون وشديد القلوية وله رائحة مميزة. تعتمد ذوبان هيدروكسيد الأمونيوم في الماء على درجة الحرارة والتركيز، مع ارتفاع درجات الحرارة والتركيزات مما يؤدي إلى زيادة الذوبان.
ما هي الصيغة الكيميائية لهيدروكسيد الأمونيوم؟
الصيغة الكيميائية لهيدروكسيد الأمونيوم هي NH4OH.
ما هي صيغة هيدروكسيد الأمونيوم؟
صيغة هيدروكسيد الأمونيوم هي NH4OH.
هل هيدروكسيد الأمونيوم قاعدة قوية؟
نعم، يعتبر هيدروكسيد الأمونيوم قاعدة قوية. وهو يتفكك تمامًا في الماء لتكوين أيونات الهيدروكسيد (OH-) وأيونات الأمونيوم (NH4+)، مما يجعله قلويًا للغاية مع درجة حموضة تبلغ حوالي 11. هذه القلوية العالية تجعله مادة كيميائية مفيدة في مختلف التطبيقات الصناعية والمنزلية، مثل التنظيف والتطهير. تعديل الرقم الهيدروجيني. ومع ذلك، من المهم التعامل مع هيدروكسيد الأمونيوم بحذر، لأنه يمكن أن يكون مسببًا للتآكل وخطيرًا إذا لم يتم التعامل معه بشكل صحيح.
الاسم المركب nh4oh
اسم المركب الكيميائي لـ NH4OH هو هيدروكسيد الأمونيوم.
اسم nh4oh
اسم NH4OH هو هيدروكسيد الأمونيوم.
