رابع كلوريد الكربون سائل عديم اللون ذو رائحة حلوة. وكان يستخدم بشكل شائع كمذيب، لكن إنتاجه واستخدامه انخفض بسبب آثاره الصحية والبيئية الضارة.
| اسم الأيوباك | رباعي كلورو ميثان |
| الصيغة الجزيئية | CCl4 |
| CAS رقم | 56-23-5 |
| المرادفات | رباعي الكربون، تيترافورم، بيركلوروميثان، تيتراسول |
| إنتشي | InChI=1S/CCl4/c2-1(3,4)5 |
خصائص رابع كلوريد الكربون
صيغة رابع كلوريد الكربون
الصيغة الكيميائية لرابع كلوريد الكربون هي CCl4. وهو يمثل جزيءًا يتكون من ذرة كربون مرتبطة بأربع ذرات كلور. توفر الصيغة معلومات أساسية حول التركيب العنصري وترتيب الذرات داخل المركب.
رابع كلوريد الكربون الكتلة المولية
يتم حساب الكتلة المولية لرباعي كلورو ميثان عن طريق إضافة الكتل الذرية للعناصر المكونة له. تبلغ الكتلة المولية للكربون 12.01 جم / مول، بينما تبلغ الكتلة المولية للكلور 35.45 جم / مول. وبجمع هذه القيم معًا، تصبح الكتلة المولية لرباعي كلورو ميثان حوالي 153.82 جم/مول.
نقطة غليان رابع كلوريد الكربون
يحتوي رباعي كلورو الميثان على نقطة غليان عالية نسبيًا تبلغ 76.72 درجة مئوية (170.1 درجة فهرنهايت). وهذا يعني أنه عند الضغط الجوي القياسي، يتغير المركب من سائل إلى غاز عند درجة الحرارة تلك. تعكس نقطة الغليان قوة القوى الجزيئية داخل المادة.
نقطة انصهار رابع كلوريد الكربون
نقطة انصهار رباعي كلورو الميثان هي -22.92 درجة مئوية (-9.26 درجة فهرنهايت). هذه هي درجة الحرارة التي يتحول عندها الشكل الصلب للمركب إلى سائل. توفر نقطة الانصهار نظرة ثاقبة على قوة الروابط التي تربط الذرات معًا داخل الشبكة البلورية.
كثافة رابع كلوريد الكربون جم/مل
تبلغ كثافة رباعي كلورو الميثان حوالي 1.586 جم / مل. تشير الكثافة إلى كتلة المادة لكل وحدة حجم. تشير كثافة رباعي كلورو الميثان إلى أنه أكثر كثافة من الماء الذي تبلغ كثافته 1 جم/مل.
الوزن الجزيئي لرابع كلوريد الكربون
يتم حساب الوزن الجزيئي لرباعي كلورو الميثان عن طريق إضافة الأوزان الذرية للذرات المكونة له. مع ذرة كربون واحدة (12.01 جم/مول) وأربع ذرات كلور (35.45 جم/مول لكل منها)، يبلغ الوزن الجزيئي لرباعي كلورو ميثان حوالي 153.82 جم/مول.
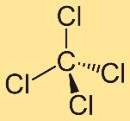
هيكل رابع كلوريد الكربون
يتكون هيكل رباعي كلورو الميثان من ذرة كربون مركزية مرتبطة بأربع ذرات كلور. يتم وضع ذرات الكلور هذه بشكل متناظر حول ذرة الكربون، لتشكل هندسة رباعية السطوح. يساهم هذا الهيكل في خصائص وسلوك المركب.
ذوبان رابع كلوريد الكربون
رباعي كلورو الميثان قليل الذوبان في الماء، حيث تبلغ قابلية ذوبانه حوالي 0.8 جم / لتر عند 20 درجة مئوية. ومع ذلك، فإنه يظهر قابلية ذوبان أعلى في المذيبات العضوية مثل الإيثانول والأثير والبنزين. تتأثر خصائص الذوبان بالقوى الجزيئية وقطبية المواد المعنية.
| مظهر | سائل عديم اللون |
| جاذبية معينة | 1,586 |
| لون | لا يوجد |
| يشم | ناعم |
| الكتلة المولية | 153.82 جرام/مول |
| كثافة | 1,586 جم/مل |
| نقطة الانصهار | -22.92 درجة مئوية (-9.26 درجة فهرنهايت) |
| نقطة الغليان | 76.72 درجة مئوية (170.1 درجة فهرنهايت) |
| نقطة فلاش | لا يوجد |
| الذوبان في الماء | 0.8 جم/لتر عند 20 درجة مئوية |
| الذوبان | قابل للذوبان في المذيبات العضوية مثل الإيثانول والأثير والبنزين |
| ضغط البخار | 11.9 ملم زئبق عند 20 درجة مئوية |
| كثافة بخار | 5.3 (الهواء = 1) |
| pKa | لا يوجد |
| الرقم الهيدروجيني | لا يوجد |
سلامة ومخاطر رابع كلوريد الكربون
يشكل رابع كلورو الميثان مخاطر كبيرة على السلامة. تعتبر شديدة السمية ويمكن أن تضر بصحة الإنسان بشكل خطير. استنشاق أبخرةه يمكن أن يسبب تهيج الجهاز التنفسي، والدوخة، والغثيان، وحتى تلف الكبد والكلى. قد يؤدي ملامسة الجلد للسائل إلى حدوث حروق وتهيج. ويعتبر المركب أيضًا مادة مسرطنة معروفة، مما يشكل مخاطر صحية على المدى الطويل. وبالإضافة إلى ذلك، يشكل رباعي كلورو الميثان خطراً على البيئة، مع احتمال تلويث التربة والمياه. وبسبب هذه المخاطر، تم تقييد إنتاجه واستخدامه بشكل كبير من أجل تقليل التعرض له وحماية صحة الإنسان والبيئة. وينبغي اتباع بروتوكولات المناولة والتخزين والتخلص المناسبة للتخفيف من المخاطر المرتبطة برابع كلورو الميثان.
| رموز الخطر | تي، اكسن |
| وصف الأمان | سام جدا؛ ضار |
| أرقام تعريف الأمم المتحدة | أ 1846 |
| رمز النظام المنسق | 2903.14.0000 |
| فئة الخطر | 6.1 (المواد السامة) |
| مجموعة التعبئة | ثانيا |
| تسمم | سمية حادة، مسرطنة |
طرق تصنيع رابع كلوريد الكربون
يمكن تصنيع رباعي كلورو الميثان بطرق مختلفة. تتضمن الطريقة الشائعة التفاعل بين غاز الكلور (Cl2) وثاني كبريتيد الكربون (CS2) في وجود محفز مثل كلوريد الألومنيوم (AlCl3).
في هذه العملية، يتفاعل غاز الكلور مع بخار ثاني كبريتيد الكربون لإنتاج رباعي كلورو الميثان والكبريت. يستمر التفاعل على النحو التالي:
Cl2 + CS2 → CCl4 + S
هناك طريقة أخرى تتضمن التفاعل بين الميثان (CH4) وغاز الكلور. في ظل ظروف خاضعة للرقابة، يتفاعل الميثان مع الكلور في وجود الضوء فوق البنفسجي أو الحرارة لإنتاج رباعي كلورو الميثان وكلوريد الهيدروجين. يستمر التفاعل على النحو التالي:
CH4 + 4Cl2 → CCl4 + 4HCl
كلورة ثاني كبريتيد الكربون باستخدام كلوريد الهيدروجين (HCl) حيث ينتج عامل الكلورة رباعي كلورو ميثان. يتطلب هذا التفاعل وجود محفز، مثل كلوريد الحديد (III) (FeCl3). يستمر التفاعل على النحو التالي:
CS2 + 3HCl + FeCl3 → CCl4 + S + 2FeCl2
عند تصنيع رباعي كلورو الميثان، يجب على الأفراد توخي الحذر بسبب الطبيعة الخطرة للمركب. ويجب عليهم استخدام تدابير السلامة الصارمة والمعدات المناسبة لضمان رفاهيتهم ومنع التلوث البيئي.
استخدامات رابع كلوريد الكربون
استخدمت العديد من التطبيقات الخصائص الفريدة لرباعي كلورو الميثان. وهذه بعض استخداماته:
- المذيب: يقوم رابع كلورو ميثان بإذابة الزيوت والشحوم والمطاط والشموع، ويعمل كمذيب. ومع ذلك، فقد أدت سميته والمخاوف البيئية إلى تقليل استخدامه للمذيبات بشكل كبير.
- طفاية الحريق: رباعي كلورو الميثان يستخدم لإطفاء أنواع معينة من حرائق الأجهزة الكهربائية والسوائل القابلة للاشتعال. وقد أدت البدائل الأكثر أمانًا وآثارها الضارة إلى التخلي التدريجي عن استخدامها.
- الوسيط الكيميائي: يعمل رباعي كلورو الميثان كمادة كيميائية وسيطة في إنتاج مركبات مختلفة، مثل المبردات والمبيدات الحشرية والمستحضرات الصيدلانية.
- عامل التنظيف: استخدمت الصناعات سابقًا رباعي كلورو الميثان كعامل تنظيف للأسطح المعدنية والمكونات الإلكترونية. ومع ذلك، فقد دفعت المخاطر الصحية والبيئية إلى تفضيل البدائل الأكثر أمانًا.
- كاشف المختبر: يستخدم رباعي كلورو الميثان أحيانًا ككاشف أو مذيب لتفاعلات واستخراجات معينة في المختبر. يفضل الكيميائيون عمومًا البدائل الأكثر أمانًا ويحدون من استخدامها.
ومن الأهمية بمكان أن نلاحظ أن العديد من هذه التطبيقات قد انخفضت، أو حتى توقفت تمامًا، بسبب الآثار الضارة لرباعي كلورو الميثان على صحة الإنسان والبيئة. ونتيجة لذلك، انخفض استخدام رباعي كلورو الميثان بشكل كبير، وتم اعتماد مواد بديلة أقل سمية وأقل تأثيراً على البيئة في مختلف الصناعات.
أسئلة:
س: هل لا يزال بإمكانك شراء بدائل لرابع كلوريد الكربون؟
ج: نعم، هناك بدائل لرباعي كلورو الميثان أكثر أمانًا ولها تأثير أقل على البيئة.
س: هل لا يزال بإمكانك شراء رابع كلوريد الكربون؟
ج: إن رباعي كلورو الميثان محظور في العديد من البلدان بسبب سميته ومخاطره البيئية، وبالتالي فإن توفره للشراء محدود.
س: هل رابع كلوريد الكربون قانوني؟
ج: يخضع رباعي كلورو الميثان لقيود قانونية في العديد من البلدان بسبب آثاره الضارة على الصحة والبيئة.
س: هل رابع كلوريد الكربون قلوي أم حمضي؟
ج: رباعي كلورو الميثان ليس قلوياً ولا حمضياً؛ إنه مركب محايد.
س: هل رابع كلوريد الكربون قطبي أم غير قطبي؟
ج: رباعي كلورو الميثان هو جزيء غير قطبي بسبب تركيبه رباعي السطوح المتماثل، مما يؤدي إلى المشاركة المتساوية للإلكترونات.
س: ما هي الكتلة المولية لرابع كلوريد الكربون؟
ج: تبلغ الكتلة المولية لرباعي كلورو ميثان حوالي 153.82 جم/مول.
س: ما هو رابع كلوريد الكربون؟
ج: رباعي كلورو الميثان هو مركب سائل عديم اللون يستخدم في المقام الأول كمذيب في الماضي، ولكن استخدامه أصبح الآن محدودًا بسبب سميته والمخاوف البيئية.
س: ما الصيغة الكيميائية لرابع كلوريد الكربون؟
ج: الصيغة الكيميائية لرباعي كلورو الميثان هي CCl4.
س: هل الرابطة موجودة في رابع كلوريد الكربون؟
ج: الرابطة في رباعي كلورو الميثان تساهمية، حيث توجد أربع روابط تساهمية بين ذرة الكربون المركزية وذرات الكلور المحيطة بها.
س: هل رابع كلوريد الكربون أيوني أم تساهمي؟
ج: رباعي كلورو الميثان مركب تساهمي لأنه يشكل روابط عن طريق مشاركة الإلكترونات بين ذرات الكربون والكلور.
س: ما عدد ذرات الكلور الموجودة في جزيء رابع كلوريد الكربون؟
ج: هناك أربع ذرات كلور في جزيء رباعي كلورو ميثان.
س: حدد المذيب الأفضل لكل مادة مذابة: الماء أم رابع كلوريد الكربون؟
ج: يعتمد المذيب الأفضل على المذاب. يعتبر الماء بشكل عام مذيبًا أفضل للمواد القطبية، في حين أن رباعي كلورو الميثان أفضل للمواد غير القطبية.
س: تركيب لويس لرباعي كلورو الميثان؟
ج: في بنية لويس لرباعي كلورو الميثان، ترتبط ذرة الكربون المركزية بأربع ذرات كلور، مع عدم وجود أزواج وحيدة على ذرة الكربون المركزية.
