بروميد النحاس (CuBr2) هو مركب يتكون من النحاس والبروم. إنه يظهر اللون الأزرق والأخضر، وغالبا ما يستخدم في التخليق العضوي وكمحفز لحمض لويس.
| اسم الأيوباك | بروميد النحاس الثنائي |
| الصيغة الجزيئية | CuBr2 |
| CAS رقم | 7789-45-9 |
| المرادفات | بروميد النحاسيك، ثنائي بروميد النحاس |
| إنتشي | InChI=1S/Br2.Cu |
خصائص بروميد النحاس
صيغة بروميد النحاس
صيغة بروميد النحاسيك هي CuBr2. وهو يمثل مركبًا مكونًا من ذرة نحاس واحدة وذرتين من البروم. وينتج عن هذا المزيج مادة بلورية زرقاء وخضراء، تستخدم عادة في التفاعلات الكيميائية المختلفة.
بروميد النحاس الكتلة المولية
تبلغ الكتلة المولية لبروميد النحاسيك حوالي 223.36 جرامًا لكل مول. يتم الحصول على هذه القيمة عن طريق إضافة الكتل الذرية لذرة نحاس واحدة (Cu) وذرتين من البروم (Br) الموجودة في الصيغة CuBr2.
نقطة غليان بروميد النحاس
بروميد النحاسيك لديه نقطة غليان تبلغ حوالي 1294 درجة مئوية (حوالي 2361 درجة فهرنهايت). تشير درجة الحرارة هذه إلى النقطة التي تتغير عندها المادة من السائل إلى الغاز تحت الضغط الجوي القياسي.
نقطة انصهار بروميد النحاس
تبلغ نقطة انصهار بروميد النحاسيك حوالي 498 درجة مئوية (حوالي 928 درجة فهرنهايت). تمثل درجة الحرارة هذه النقطة التي تتحول عندها المادة الصلبة إلى الحالة السائلة عند تسخينها.
كثافة بروميد النحاس جم/مل
تبلغ كثافة بروميد النحاسيك حوالي 4.71 جرام لكل مليلتر (جم / مل) عند درجة حرارة الغرفة القياسية والضغط الجوي. تكشف هذه القيمة عن مقدار الكتلة الموجودة لكل وحدة حجم من المادة.
الوزن الجزيئي لبروميد النحاس
يبلغ الوزن الجزيئي لبروميد النحاسيك حوالي 223.36 جرامًا لكل مول. تعتبر هذه القيمة حاسمة بالنسبة للحسابات الكيميائية المختلفة وتعمل كمرجع لكمية المادة الموجودة في عينة معينة.
هيكل بروميد النحاس
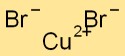
يحتوي بروميد النحاسيك على بنية شبكية بلورية تكون فيها ذرات النحاس محاطة بذرات البروم والعكس صحيح. يشكل هذا الترتيب نمطًا مستقرًا ومنظمًا، مما يساهم في الخواص الفيزيائية للمركب.
ذوبان بروميد النحاس
بروميد النحاسيك له قابلية محدودة للذوبان في الماء. وهو أكثر قابلية للذوبان في المذيبات العضوية. تعتمد القابلية للذوبان على عوامل مثل درجة الحرارة وطبيعة المذيب المستخدم. يعد فهم قابليته للذوبان أمرًا حيويًا لمختلف التطبيقات في الكيمياء والصناعة.
| مظهر | بلورات زرقاء وخضراء |
| جاذبية معينة | غير متاح |
| لون | أزرق أخضر |
| يشم | عديم الرائحة |
| الكتلة المولية | 223.36 جرام/مول |
| كثافة | 4.71 جم/مل |
| نقطة الانصهار | 498 درجة مئوية (928 درجة فهرنهايت) |
| نقطة الغليان | 1294 درجة مئوية (2361 درجة فهرنهايت) |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | ذوبان محدود |
| الذوبان | قابل للذوبان في المذيبات العضوية مثل الإيثانول والأثير والبنزين |
| ضغط البخار | غير متاح |
| كثافة بخار | غير متاح |
| pKa | غير متاح |
| الرقم الهيدروجيني | غير متاح |
سلامة ومخاطر بروميد النحاس
يطرح بروميد النحاسيك اعتبارات معينة تتعلق بالسلامة والمخاطر. من الضروري التعامل مع هذا المركب بحذر بسبب سميته المحتملة وخصائصه المهيجة. الاتصال المباشر مع الجلد أو العينين قد يسبب تهيجًا وعدم الراحة. استنشاق غبارها أو أبخرةها يمكن أن يهيج الجهاز التنفسي. ولذلك، ينبغي ارتداء معدات الحماية الشخصية المناسبة، مثل القفازات والنظارات الواقية، عند العمل مع بروميد النحاسيك. بالإضافة إلى ذلك، يجب تخزينه بعيدًا عن المواد غير المتوافقة لتجنب التفاعلات المحتملة. في حالة الابتلاع أو التعرض العرضي، اطلب العناية الطبية على الفور. يعد الامتثال لاحتياطات السلامة أمرًا بالغ الأهمية لضمان التعامل الآمن مع بروميد النحاسيك واستخدامه.
| رموز الخطر | مهيج، تآكل |
| وصف الأمان | التعامل مع الودائع. تجنب الاتصال المباشر مع الجلد والعينين. استخدم معدات الحماية المناسبة. |
| أرقام تعريف الأمم المتحدة | غير متاح |
| رمز النظام المنسق | غير متاح |
| فئة الخطر | مهيج |
| مجموعة التعبئة | غير متاح |
| تسمم | قد يسبب تهيج الجلد والعين. استنشاق الغبار أو الأبخرة قد يؤدي إلى تهيج الجهاز التنفسي. |
طرق تصنيع بروميد النحاس
هناك عدة طرق لتصنيع بروميد النحاسيك (CuBr2). يتضمن النهج الشائع الجمع المباشر بين النحاس المعدني أو أكسيد النحاس مع حمض الهيدروبروميك . في هذه الطريقة نضيف النحاس إلى الحمض، فيخضع لتفاعل كيميائي ينتج عنه تكوين بروميد النحاسيك وإطلاق غاز الهيدروجين.
طريقة أخرى هي التفاعل بين كربونات النحاس أو هيدروكسيد النحاس مع حمض الهيدروبروميك. تتفاعل الكربونات أو الهيدروكسيد مع الحمض لإنتاج بروميد النحاسيك والماء وثاني أكسيد الكربون.
بالإضافة إلى ذلك، لتصنيع بروميد النحاسيك، يمكن استخدام تفاعل الإزاحة المزدوج. تتضمن هذه الطريقة التفاعل بين ملح النحاس القابل للذوبان، مثل كبريتات النحاس، وملح بروميد قابل للذوبان، مثل بروميد الصوديوم. يؤدي التفاعل إلى تكوين بروميد النحاسيك وملح قابل للذوبان من المعدن أو شبه الفلز الآخر الموجود في التفاعل.
بالإضافة إلى ذلك، لتصنيع بروميد النحاسيك، يمكننا استخدام الطرق الكهروكيميائية. تتضمن هذه الطرق استخدام خلية كهروكيميائية ذات أقطاب نحاسية ومصدر أيون البروميد. عندما نطبق تيارًا كهربائيًا، يتشكل بروميد النحاسيك على أحد القطبين، بينما ينطلق غاز البروم على القطب الآخر.
يعتمد اختيار طريقة التوليف على عوامل مثل توفر الكواشف، والنقاء المطلوب، ومدى التفاعل. يجب مراعاة احتياطات المعالجة والسلامة المناسبة أثناء جميع الإجراءات الاصطناعية.
استخدامات بروميد النحاس
يجد بروميد النحاس (CuBr2) تطبيقات متعددة الاستخدامات في مختلف الصناعات نظرًا لخصائصه الفريدة. فيما يلي بعض استخداماته البارزة:
- التخليق العضوي : يعمل بروميد النحاسيك كمحفز في العديد من التفاعلات العضوية، مثل اقتران أولمان وتفاعل فورتز-فيتيج، مما يسمح بتكوين روابط كربون-كربون وروابط كربون-ذرة مغايرة.
- التصوير الفوتوغرافي : يستخدم في عمليات التصوير الفوتوغرافي لتحسس المستحلبات وتحسين حساسية الأفلام والألواح مما يسهل التقاط صور عالية الجودة.
- الطلاء الكهربائي : يستخدم بروميد النحاس في عمليات الطلاء الكهربائي لترسيب طبقات من النحاس على الأسطح، مما يوفر مقاومة للتآكل وتشطيبات زخرفية.
- صناعة أشباه الموصلات : في قطاع الإلكترونيات، يتم استخدامه في تصنيع البلورات النانوية القائمة على بروميد النحاسيك، والتي لها تطبيقات في الإلكترونيات الضوئية والضوئيات.
- صبغ اللهب : يستخدم بروميد النحاس في الألعاب النارية والألعاب النارية لإنتاج لون لهب أخضر، مما يضيف جاذبية بصرية إلى شاشات العرض.
- الطب : على الرغم من محدوديته، فقد تم استكشافه لتطبيقات علاجية محتملة بسبب خصائصه المضادة للبكتيريا.
- تكنولوجيا الليزر : يتم استخدام ليزر بروميد النحاس في الأبحاث العلمية ودراسات التألق المستحث بالليزر ولتوليد نبضات ليزر عالية الطاقة.
- التحليل الكيميائي : يستخدم في الكيمياء التحليلية للتحليلات النوعية والكمية.
- تفاعلات المعالجة بالبروم : يعمل بروميد النحاسيك كعامل للبرومة، مما يسهل إضافة البروم إلى المركبات العضوية.
- الطباعة الحجرية : في عمليات الطباعة الحجرية، تم دراسة مركبات بروميد النحاس لاستخدامها في تقنيات التصنيع الدقيقة والنانوية.
تثبت التطبيقات المختلفة لبروميد النحاسيك أهميته في مختلف المجالات، مما يجعله مركبًا قيمًا في المساعي الصناعية والعلمية.
أسئلة:
س: ما هي الكتلة المولية لبروميد النحاس الثنائي؟
ج: تبلغ الكتلة المولية لبروميد النحاس الثنائي (II) حوالي 223.36 جم/مول.
س: ما هي صيغة بروميد النحاس الثنائي؟
ج: صيغة بروميد النحاس الثنائي (II) هي CuBr2.
س: هل بروميد النحاس الثنائي قابل للذوبان في الماء؟
ج: بروميد النحاسيك (II) ذو قابلية ذوبان محدودة في الماء.
س: ما هو استخدام بروميد النحاس (II)؟
ج: يستخدم بروميد النحاس (II) كمحفز في التركيب العضوي، والتصوير الفوتوغرافي، والطلاء الكهربائي، وصناعة أشباه الموصلات.
س: هل يمكن استخدام بروميد الزنك والنحاس كبديل لمرة واحدة؟
ج: نعم، يخضع بروميد الزنك والنحاس الثنائي (II) لتفاعل استبدال واحد، مما ينتج عنه بروميد الزنك والنحاس المعدني.
س: هل يحدث تفاعل عند دمج المحاليل المائية لخلات الباريوم وبروميد النحاس الثنائي؟
ج: نعم، يحدث تفاعل ينتج عنه تكوين بروميد الباريوم وخلات النحاس الثنائي.
س: ما الأيونات، إن وجدت، التي تتكون عند إضافة بروميد النحاس الثنائي إلى الماء؟
ج: عند إضافة بروميد النحاسيك (II) إلى الماء، فإنه يتفكك إلى أيونات Cu^2+ وأيونات بروميد (Br^-).
س: هل يشكل CuBr2 رابطة أيونية؟
ج: نعم، يشكل CuBr2 رابطة أيونية بين أيونات النحاس والبروم.
س: هل يشكل CuBr2 رابطة تساهمية؟
ج: لا، CuBr2 لا يشكل رابطة تساهمية.
س: هل CuBr2 قابل للذوبان في الماء؟
ج: إن CuBr2 له قابلية ذوبان محدودة في الماء.
س: ما هو CuBr2؟
ج: CuBr2 هي الصيغة الكيميائية لبروميد النحاسيك (II)، وهو مركب بلوري أخضر مزرق.
س: هل CuBr2 قابل للذوبان أم غير قابل للذوبان؟
ج: إن CuBr2 قليل الذوبان في الماء.
س: ما هي النسبة المئوية لكتلة النحاس في CuBr2؟
ج: تبلغ نسبة كتلة النحاس في CuBr2 حوالي 47.5%.
