برمنجنات البوتاسيوم (KMnO4) هو مركب بلوري أرجواني يستخدم لمجموعة متنوعة من الأغراض، مثل تطهير المياه، وعلاج الأمراض الجلدية، وككاشف مختبري. ويمكن استخدامه أيضًا كعامل مؤكسد قوي.
| اسم الأيوباك | برمنجنات البوتاسيوم |
| الصيغة الجزيئية | KMnO4 |
| CAS رقم | 7722-64-7 |
| المرادفات | برمنجنات البوتاس، بلورات كوندي، معدن الحرباء، هايبرمنجان، كاليوم هايبرمنجانيكوم |
| إنتشي | InChI=1S/K.Mn.4O/q+1;;;;-1 |
خصائص برمنجنات البوتاسيوم
صيغة برمنجنات البوتاسيوم
الصيغة الكيميائية لبرمنجنات البوتاسيوم هي KMnO4. ويتكون من أيون البوتاسيوم (K+)، وأيون المنغنيز (MnO4^-) وأربع ذرات أكسجين (O). تشير الصيغة إلى نوع وعدد الذرات التي يتكون منها المركب. يتم استخدامه لكتابة المعادلات الكيميائية وحساب كتلة وعدد الذرات الموجودة في كمية معينة من المادة.
برمنجنات البوتاسيوم الكتلة المولية
KMnO4 له كتلة مولية تبلغ 158,034 جم/مول. وهذا يعني أن المول الواحد من KMnO4، والذي يعادل 6.022 × 10^23 جزيء، لديه كتلة 158.034 جرامًا. يتم حساب الكتلة المولية للمركب عن طريق جمع الكتل الذرية لجميع العناصر الموجودة في المركب. في حالة KMnO4، يتم حساب الكتلة المولية عن طريق إضافة الكتل الذرية للبوتاسيوم والمنغنيز والأكسجين.
نقطة غليان برمنجنات البوتاسيوم
ليس لدى KMnO4 نقطة غليان محددة لأنه يتحلل قبل أن يصل إلى نقطة الغليان. عند الضغط الجوي، يبدأ KMnO4 في التحلل عند حوالي 240 درجة مئوية. عند تسخينه، يطلق الأكسجين أولاً ويشكل منجنات البوتاسيوم، والذي يتحلل بعد ذلك إلى أكسيد البوتاسيوم وأكسيد المنغنيز.
نقطة انصهار برمنجنات البوتاسيوم
KMnO4 لديه نقطة انصهار عالية تبلغ 240 درجة مئوية. وهذا يعني أنه عند درجات حرارة أقل من 240 درجة مئوية، سوف يتواجد KMnO4 في حالة صلبة. عند تسخينه، يخضع KMnO4 لسلسلة من التغيرات الكيميائية، بما في ذلك إطلاق الأكسجين وتكوين أكاسيد المنغنيز المختلفة.
كثافة برمنجنات البوتاسيوم جم/مل
تبلغ كثافة KMnO4 2.703 جم/مل عند درجة حرارة الغرفة. وهذا يعني أن الملليلتر الواحد من KMnO4 يزن 2.703 جرام. كثافة المادة هي نسبة كتلتها إلى حجمها. وفي حالة KMnO4، فإن كثافته العالية تجعله مفيدًا في فصله عن المواد الأخرى عن طريق الترشيح.
الوزن الجزيئي لبرمنجنات البوتاسيوم
الوزن الجزيئي لـ KMnO4 هو 158.034 جم/مول. تمثل هذه القيمة متوسط كتلة جزيء KMnO4. يتم حسابه عن طريق إضافة الكتل الذرية للبوتاسيوم والمنغنيز والأكسجين التي يتكون منها المركب.
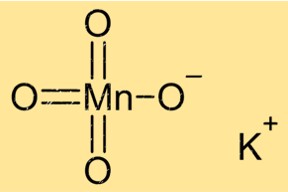
هيكل برمنجنات البوتاسيوم
يحتوي KMnO4 على بنية بلورية ذات نظام بلوري أحادي الميل. بلوراته أرجوانية اللون ولها شكل منشوري. يحتوي المركب على هندسة تنسيق ثماني السطوح، مع ست ذرات أكسجين تحيط بذرة المنغنيز المركزية. توجد أيونات البوتاسيوم بين طبقات ذرات المنغنيز والأكسجين.
| مظهر | مادة صلبة بلورية أرجوانية داكنة |
| جاذبية معينة | 2,703 جم/سم3 |
| لون | الأرجواني الداكن |
| يشم | عديم الرائحة |
| الكتلة المولية | 158,034 جم/مول |
| كثافة | 2,703 جم/سم3 |
| نقطة الانصهار | 240 درجة مئوية |
| نقطة الغليان | ينهار قبل الغليان |
| نقطة فلاش | غير قابل للتطبيق |
| الذوبان في الماء | 6.38 جم/لتر عند 20 درجة مئوية |
| الذوبان | قابل للذوبان في الماء، الإيثانول، الأسيتون |
| ضغط البخار | غير قابل للتطبيق |
| كثافة بخار | غير قابل للتطبيق |
| pKa | 2.17 |
| الرقم الهيدروجيني | 7.2 – 8.9 (محلول 1%) |
سلامة ومخاطر برمنجنات البوتاسيوم
يمكن أن يكون KMnO4 خطيرًا إذا لم يتم التعامل معه بشكل صحيح. وهو عامل مؤكسد قوي يمكن أن يتفاعل بعنف مع عوامل الاختزال والمركبات العضوية والمواد الكيميائية الأخرى. قد يسبب تهيجًا للجلد والعينين وقد يكون ضارًا في حالة ابتلاعه أو استنشاقه. قد يؤدي المركب أيضًا إلى تلطيخ الجلد والملابس. وينبغي اتخاذ احتياطات السلامة المناسبة عند التعامل مع KMnO4، بما في ذلك ارتداء الملابس الواقية والنظارات والقفازات. يجب أن يتم تخزينه في منطقة باردة وجافة وجيدة التهوية بعيدا عن المواد غير المتوافقة. في حالة تعرضها أو ابتلاعها، اطلب العناية الطبية على الفور.
| رموز الخطر | يا، اكس.ن |
| وصف الأمان | S22، S26، S36/37/39، S45 |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 1490 |
| رمز النظام المنسق | 28416100 |
| فئة الخطر | 5.1 |
| مجموعة التعبئة | ثانيا |
| تسمم | سام إذا تم ابتلاعه أو استنشاقه. قد يسبب تهيج الجلد والعين. |
طرق تصنيع برمنجنات البوتاسيوم
يمكن لطرق مختلفة تصنيع KMnO4.
تتضمن إحدى الطرق تفاعل ثاني أكسيد المنغنيز مع هيدروكسيد البوتاسيوم وعامل مؤكسد، مثل الكلور أو بيروكسيد الهيدروجين.
تتضمن الطريقة الأخرى تفاعل منجنات البوتاسيوم مع غاز الكلور .
هناك طريقة أخرى تتضمن تفاعل هيدروكسيد البوتاسيوم مع ثاني أكسيد المنغنيز ثم أكسدة الخليط الناتج بعامل مؤكسد.
تتضمن عملية التخليق عادة تسخين المواد المتفاعلة إلى درجة حرارة معينة والحفاظ على درجة الحرارة لفترة معينة. وتتكون العملية من تصفية الخليط الناتج والحصول على KMnO4 عن طريق التبلور.
استخدامات برمنجنات البوتاسيوم
يستخدم KMnO4 في العديد من الصناعات بسبب خصائصه المؤكسدة القوية. فيما يلي بعض الاستخدامات الشائعة لـ KMnO4:
- معالجة المياه: تستخدم لمعالجة المياه للأغراض البلدية والصناعية، حيث يمكنها إزالة الشوائب والقضاء على الروائح الكريهة.
- التطبيقات الطبية: يستخدم موضعياً لعلاج الأمراض الجلدية (الأكزيما والتهاب الجلد والالتهابات الفطرية).
- الاستخدام المعملي: يستخدم كعامل مؤكسد في التجارب المعملية المختلفة وكصبغة في علم الأحياء لإبراز الخلايا والأنسجة.
- الزراعة: يستخدم كمبيد للفطريات والبكتيريا لحماية المحاصيل من الآفات والأمراض الضارة.
- الكيمياء: تستخدم في الكيمياء التحليلية لتحديد تركيز بعض المواد الكيميائية وفي الكيمياء العضوية ككاشف في التفاعلات الكيميائية.
- مكافحة الحرائق: يستخدم كمثبط للهب ولإطفاء أنواع معينة من الحرائق.
- التطبيقات الصناعية: تستخدم في إنتاج المواد الكيميائية والمنسوجات والبطاريات.
أسئلة:
س: ما هو الغاز الذي ينطلق عند تحلل برمنجنات البوتاسيوم؟
ج: عند تحلل KMnO4، يتحرر غاز الأكسجين (O2).
س: ما هو برمنجنات البوتاسيوم؟
ج: برمنجنات البوتاسيوم عامل مؤكسد قوي صيغته الكيميائية KMnO4.
س: ما هي الصيغة الكيميائية لبرمنجنات البوتاسيوم؟
ج: الصيغة الكيميائية لبرمنجنات البوتاسيوم هي KMnO4.
س: أين يمكن شراء بلورات برمنجنات البوتاسيوم؟
ج: يمكن شراء بلورات KMnO4 من موردي المواد الكيميائية وشركات توريد المختبرات وتجار التجزئة عبر الإنترنت.
س: ما هو KMnO4؟
ج: KMnO4 هي الصيغة الكيميائية لبرمنجنات البوتاسيوم.
س: ما هو عدد تأكسد المنغنيز في KMnO4؟
ج: عدد تأكسد المنغنيز في KMnO4 هو +7.
س: ما هو عدد تأكسد الأكسجين في KMnO4؟
ج: عدد تأكسد الأكسجين في KMnO4 هو -2.
س: ما عدد المولات الموجودة في 25.0 جرامًا من KMnO4؟
ج: لحساب عدد المولات في 25.0 جرام من KMnO4، علينا قسمة الكتلة المعطاة على الكتلة المولية لـ KMnO4. الكتلة المولية لـ KMnO4 هي 158.034 جم/مول. ولذلك، يوجد ما يقرب من 0.158 مول من KMnO4 في 25.0 جرام.
