أسيتوفينون أو ميثيل فينيل كيتون هو مركب عضوي عطري له الصيغة C8H8O. يتم استخدامه في إنتاج العطور والراتنجات، وكمذيب ووسيط في الأدوية.
| اسم الأيوباك | 1-فينيليثانون |
| الصيغة الجزيئية | C8H8O |
| CAS رقم | 98-86-2 |
| المرادفات | ميثيل فينيل كيتون، فينيل ميثيل كيتون، AP، أسيتيل بنزين، بنزويل ميثيل، إيثيل فينيل كيتون، هيبنون |
| إنتشي | إنتشي = 1S/C8H8O/c1-7(9)8-5-3-2-4-6-8/h2-6H,1H3 |
هيكل الأسيتوفينون
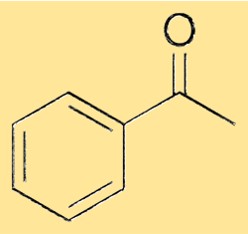
يتكون هيكل الأسيتوفينون من مجموعة فينيل مرتبطة بمجموعة كربونيل عبر رابطة واحدة. تتكون مجموعة الكربونيل من ذرة كربون مرتبطة بشكل مزدوج بذرة الأكسجين. مجموعة الفينيل عبارة عن حلقة مكونة من ستة أعضاء من ذرات الكربون مع خمس ذرات هيدروجين متصلة بها، وتحتل ذرة الكربونيل الكربونيل المركز السادس. يمنح هذا الهيكل الأسيتوفينون خصائصه المميزة ويسمح له بالعمل كمادة خام متعددة الاستخدامات لتخليق مجموعة متنوعة من المواد الكيميائية.
نقطة انصهار الأسيتوفينون
الأسيتوفينون لديه نقطة انصهار -15.7 درجة مئوية. نقطة الانصهار هي درجة الحرارة التي تتحول عندها المادة الصلبة إلى سائل عند ضغط ثابت. الأسيتوفينون هو مادة صلبة بلورية في درجة حرارة الغرفة وله نقطة انصهار منخفضة نسبيًا مقارنة بالمركبات المماثلة الأخرى. يتم تحديد نقطة انصهار المركب من خلال تركيبه الجزيئي وقوة قوى الجزيئات بينه.
طيف الأشعة تحت الحمراء من الأسيتوفينون
يُظهر طيف الأشعة تحت الحمراء للأسيتوفينون قممًا مميزة عند 1705 سم^-1، وهو ما يتوافق مع مجموعة الكربونيل، وعند 3030-3100 سم^-1، والذي يتوافق مع تمدد CH العطري. توفر هذه القمم معلومات مهمة بخصوص المجموعات الوظيفية الموجودة في الجزيء.
الكتلة المولية للأسيتوفينون:
يحتوي الأسيتوفينون على كتلة مولية تبلغ 120.15 جم / مول. وهو مركب عضوي عطري يحتوي على مجموعة كربونيل متصلة بحلقة فينيل. الكتلة المولية هي مجموع الكتل الذرية للذرات الموجودة في مول واحد من المركب. في حالة الأسيتوفينون، فهو يحتوي على 8 ذرات كربون و8 ذرات هيدروجين وذرة أكسجين واحدة، مما يعطي إجمالي 17 ذرة في الجزيء. الكتلة المولية هي خاصية مهمة للمركب لأنها تستخدم لحساب كمية المادة في عينة معينة، وهو أمر ضروري لمختلف التطبيقات في الكيمياء والصناعة.
نقطة غليان الأسيتوفينون
درجة غليان الأسيتوفينون هي 202 درجة مئوية. نقطة الغليان هي درجة الحرارة التي يتحول عندها السائل إلى غاز عند ضغط ثابت. الأسيتوفينون هو مركب عضوي متطاير وله نقطة غليان عالية نسبيًا مقارنة بالمركبات المماثلة الأخرى. يتم تحديد نقطة غليان المركب من خلال قوة القوى بين الجزيئات، وهي القوى التي تربط الجزيئات معًا في الحالة السائلة أو الصلبة. في حالة الأسيتوفينون، فهو يحتوي على مجموعة كربونيل قطبية يمكنها تكوين روابط هيدروجينية مع جزيئات الأسيتوفينون الأخرى، مما يقوي القوى بين الجزيئات ويزيد من درجة الغليان.
كثافة ميثيل فينيل كيتون جم/مل
تبلغ كثافة ميثيل فينيل كيتون 1.03 جم / مل في درجة حرارة الغرفة. الكثافة هي كتلة المادة لكل وحدة حجم. ميثيل فينيل كيتون هو سائل في درجة حرارة الغرفة وله كثافة عالية نسبيًا مقارنة بالمركبات المماثلة الأخرى. يتم تحديد كثافة المركب من خلال وزنه الجزيئي وكثافة جزيئاته في حجم معين. في حالة كيتون ميثيل فينيل، فهو يتمتع بوزن جزيئي مرتفع نسبيًا وبنية جزيئية مدمجة نسبيًا، مما يجعل تعبئة جزيئاته أكثر كفاءة ويزيد من كثافته.
الوزن الجزيئي لـ ميثيل فينيل كيتون
يبلغ الوزن الجزيئي لميثيل فينيل كيتون 120.15 جم / مول. الوزن الجزيئي هو مجموع الأوزان الذرية لجميع الذرات الموجودة في الجزيء. يحتوي كيتون ميثيل فينيل على 8 ذرات كربون، و8 ذرات هيدروجين، وذرة أكسجين واحدة، مما يعطي إجمالي 17 ذرة في الجزيء. الوزن الجزيئي هو خاصية مهمة للمركب لأنه يستخدم لحساب كمية المادة في عينة معينة، وهو أمر ضروري لمختلف التطبيقات في الكيمياء والصناعة.
| مظهر | عديم اللون إلى سائل أصفر شاحب |
| جاذبية معينة | 1.028-1.031 عند 25 درجة مئوية |
| لون | عديم اللون إلى أصفر شاحب |
| يشم | حلو، زهري، معسل |
| الكتلة المولية | 120.15 جرام/مول |
| كثافة | 1.03 جم/مل عند 25 درجة مئوية |
| نقطة الانصهار | -15.7 درجة مئوية |
| نقطة الغليان | 202 درجة مئوية |
| نقطة فلاش | 78 درجة مئوية |
| الذوبان في الماء | 3.3 جم/لتر عند 25 درجة مئوية |
| الذوبان | قابل للذوبان في الكحول والأثير والكلوروفورم والبنزين |
| ضغط البخار | 0.27 ملم زئبق عند 25 درجة مئوية |
| كثافة بخار | 4.15 (الهواء = 1) |
| pKa | 10.01 |
| الرقم الهيدروجيني | غير قابل للتطبيق (كيتون ميثيل فينيل ليس حمضًا ولا قاعدة) |
سلامة ومخاطر ميثيل فينيل كيتون
يمكن أن يكون ميثيل فينيل كيتون خطيرًا إذا لم يتم التعامل معه بشكل صحيح. قد يسبب تهيج الجلد والعينين والجهاز التنفسي عند ملامسته أو استنشاقه. التعرض المباشر لتركيزات عالية من بخار ميثيل فينيل كيتون قد يسبب الصداع أو الدوخة أو الغثيان. قد يؤدي تناول ميثيل فينيل كيتون إلى تهيج الجهاز الهضمي أو القيء أو الإسهال. ميثيل فينيل كيتون هو أيضًا قابل للاشتعال ويمكن أن يشكل مخاليط متفجرة مع الهواء. يجب أن يتم تخزينه في مكان بارد وجاف وجيد التهوية بعيدا عن مصادر الاشتعال. يجب ارتداء معدات الحماية الشخصية، مثل القفازات ونظارات السلامة وجهاز التنفس، عند التعامل مع كيتون ميثيل فينيل.
| رموز الخطر | Xi: مهيج، F: شديد الاشتعال |
| وصف الأمان | S16: الابتعاد عن مصادر الاشتعال – لا تدخن، S26: في حالة ملامسة العينين، اشطفها فورًا بالكثير من الماء واستشر الطبيب، S36: ارتدي ملابس واقية مناسبة، S37: ارتدي قفازات مناسبة، S39: ارتدي ملابس مناسبة ملابس واقية. حماية الوجه |
| أرقام تعريف الأمم المتحدة | الأمم المتحدة 2319 |
| رمز النظام المنسق | 291439 |
| فئة الخطر | 3 (السوائل القابلة للاشتعال) |
| مجموعة التعبئة | ثالثا |
| تسمم | يتم تصنيف ميثيل فينيل كيتون على أنه مهيج للعين من الفئة 3 ومهيج للجلد من الفئة 4. ولا يعتبر مادة مسرطنة أو مطفرة. تبلغ الجرعة المميتة 50 عن طريق الفم (الجرعة المميتة لـ 50٪ من الأشخاص الذين تم اختبارهم) في الجرذان حوالي 3000 ملغم / كغم. ولا يعتبر خطرا بيئيا كبيرا. |
طرق تخليق ميثيل فينيل كيتون
توجد طرق مختلفة لتصنيع كيتون ميثيل فينيل.
إحدى الطرق الشائعة هي أسيلة فريدل-كرافت للبنزين مع كلوريد الأسيتيل في وجود محفز حمض لويس مثل كلوريد الألومنيوم. ينتج عن هذا التفاعل كيتون ميثيل فينيل وكلوريد الهيدروجين كمنتجات ثانوية.
هناك طريقة أخرى وهي أكسدة إيثيل بنزين باستخدام الهواء أو الأكسجين في وجود محفز معدني مثل الكوبالت أو المنغنيز. ينتج عن هذا التفاعل كيتون ميثيل فينيل وحمض الأسيتيك كمنتجات ثانوية.
يمكن تصنيع ميثيل فينيل كيتون عن طريق اختزال فينيل أسيتون باستخدام عوامل اختزال مثل بوروهيدريد الصوديوم أو هيدريد ألومنيوم الليثيوم. ينتج عن هذا التفاعل كيتون ميثيل فينيل والكحول المقابل كمنتجات ثانوية.
تتضمن الطريقة الأخرى تفاعل كلوريد البنزويل مع إيثيل بنزين في وجود محفز كلوريد الألومنيوم لإنتاج كيتون ميثيل فينيل وكلوريد الهيدروجين كمنتجات ثانوية.
استخدامات ميثيل فينيل كيتون
يستخدم ميثيل فينيل كيتون في العديد من الصناعات.
- يستخدم كيتون ميثيل فينيل على نطاق واسع كمذيب لمختلف الراتنجات واسترات السليلوز والبلاستيك.
- تستخدم صناعة المواد الغذائية ميثيل فينيل كيتون كعامل منكه، خاصة لنكهات الكرز واللوز.
- تستخدم صناعة العطور ميثيل فينيل كيتون كمادة خام لإنتاج العطور والمنتجات المعطرة الأخرى.
- يتم تصنيع مواد كيميائية مختلفة مثل الأدوية والكيماويات الزراعية والأصباغ باستخدام ميثيل فينيل كيتون.
- يعمل ميثيل فينيل كيتون كوسيط في إنتاج فينيل أسيتون، وهو مادة أولية لتخليق الأمفيتامينات.
- الكومارين، وهو عطر يستخدم في الصابون والمنظفات، يتم تصنيعه من ميثيل فينيل كيتون.
- تستخدم كواشف الكيمياء العضوية ميثيل فينيل كيتون ككاشف لتخليق المركبات المختلفة.
- يعمل ميثيل فينيل كيتون كمادة خام لإنتاج مواد كيميائية أخرى مثل الستايرين والميثيلستيرين.
بشكل عام، لدى ميثيل فينيل كيتون مجموعة واسعة من التطبيقات في مختلف الصناعات بسبب خصائصه واستخداماته المتنوعة.
أسئلة:
س: هل الأسيتوفينون قطبي؟
ج: نعم، الأسيتوفينون قطبي بسبب وجود مجموعة الكربونيل (C=O) وحلقة الفينيل، مما يخلق عزم ثنائي القطب.
س: هل البنزالديهايد أو الأسيتوفينون أكثر قطبية؟
ج: البنزالديهيد أكثر قطبية من الأسيتوفينون لأنه يمتلك عزم ثنائي قطب أعلى بسبب وجود مجموعة الألدهيد (CHO) بالإضافة إلى حلقة الفينيل.
س: طيف الأشعة تحت الحمراء من الأسيتوفينون؟
ج: يُظهر طيف الأشعة تحت الحمراء للأسيتوفينون نطاق امتصاص قوي وواسع يبلغ حوالي 1700 سم^-1، وهو ما يميز الاهتزاز الممتد للكربونيل (C=O). ويظهر أيضًا قممًا تبلغ حوالي 3000-3100 سم^-1، وهو ما يتوافق مع اهتزازات التمدد لـ CH العطرية.
س: من الأسيتوفينون إلى حمض البنزويك؟
ج: يمكن تحويل الأسيتوفينون إلى حمض البنزويك عن طريق الأكسدة باستخدام عامل مؤكسد مثل برمنجنات البوتاسيوم أو حمض الكروميك. يؤدي هذا التفاعل إلى انقسام رابطة الكربون-الكربون المجاورة لمجموعة الكربونيل، يليها أكسدة الوسيط الناتج لإنتاج حمض البنزويك.
س: من البنزين إلى الأسيتوفينون؟
ج: يمكن تحويل البنزين إلى أسيتوفينون بواسطة أسيلة فريدل كرافتس باستخدام كلوريد الأسيتيل أو أنهيدريد الأسيتيك في وجود محفز حمض لويس مثل كلوريد الألومنيوم. يؤدي هذا التفاعل إلى استبدال ذرة الهيدروجين من البنزين بمجموعة الأسيتيل (-COCH3)، يليها إعادة الترتيب لتكوين الأسيتوفينون.
