L’acide borique est une poudre blanche aux propriétés antiseptiques. Il peut être utilisé comme insecticide, fongicide ou comme ingrédient dans des collyres et des solutions antiseptiques.
| Nom UICPA | Acide borique |
| Formule moléculaire | H₃BO₃ |
| Numero CAS | 10043-35-3 |
| Synonymes | Acide boracique, acide orthoborique, trihydroxydoboron |
| InChI | InChI=1S/BH3O3/c2-1(3)4/h2-4H |
Veuillez noter que l’InChI fourni est une version simplifiée et que vous souhaiterez peut-être consulter des bases de données chimiques fiables pour des informations plus détaillées et précises.
Propriétés de l’acide borique
Formule d’acide borique
La formule de l’acide orthoborique est H₃BO₃. Il se compose de trois atomes d’hydrogène, d’un atome de bore et de trois atomes d’oxygène. La formule représente la composition de l’acide orthoborique au niveau moléculaire.
Acide Borique Masse molaire
La masse molaire de l’acide orthoborique est d’environ 61,83 grammes par mole. Il est déterminé en additionnant les masses atomiques de ses éléments constitutifs selon la formule moléculaire H₃BO₃.
Point d’ébullition de l’acide borique
L’acide orthoborique a un point d’ébullition d’environ 300 degrés Celsius (572 degrés Fahrenheit). Cette température indique le point auquel l’acide orthoborique passe d’une phase liquide à une phase gazeuse lorsqu’il est chauffé.
Point de fusion de l’acide borique
Le point de fusion de l’acide orthoborique est d’environ 170 degrés Celsius (338 degrés Fahrenheit). Cette température indique le point auquel l’acide orthoborique passe d’une phase solide à une phase liquide lorsqu’il est chauffé.
Densité d’acide borique g/mL
La densité de l’acide orthoborique est d’environ 1,44 gramme par millilitre. La densité est une mesure de la quantité de masse contenue dans un volume donné. Dans le cas de l’acide orthoborique, cette valeur représente la compacité de la substance.
Acide Borique Poids moléculaire
Le poids moléculaire de l’acide orthoborique est d’environ 61,83 grammes par mole. Il est calculé en additionnant les poids atomiques des atomes individuels dans une seule molécule d’acide orthoborique.
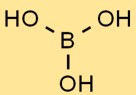
Structure de l’acide borique
L’acide orthoborique a une structure unique constituée d’atomes de bore liés à trois groupes hydroxyle (OH). Il forme un arrangement plan trigonal avec l’atome de bore au centre et les groupes hydroxyle s’étendant vers l’extérieur.
Solubilité de l’acide borique
L’acide orthoborique est modérément soluble dans l’eau. Il se dissout facilement dans l’eau, surtout lorsque l’eau est chauffée. La solubilité de l’acide orthoborique dans l’eau est influencée par des facteurs tels que la température et le pH.
| Apparence | Poudre cristalline blanche |
| Gravité spécifique | 1,435 g/cm³ |
| Couleur | Incolore |
| Odeur | Inodore |
| Masse molaire | 61,83 g/mole |
| Densité | 1,44 g/ml |
| Point de fusion | 170 °C (338 °F) |
| Point d’ébullition | 300 °C (572 °F) |
| Point d’éclair | N’est pas applicable |
| Solubilité dans l’eau | 25 g/L à 20 °C |
| Solubilité | Soluble dans les solvants tels que l’alcool, le glycérol |
| Pression de vapeur | 0,001 mmHg à 25 °C |
| Densité de vapeur | N’est pas applicable |
| pKa | 9.14 |
| pH | Environ 5,1 (solution 0,1 M) |
Veuillez noter que ces valeurs sont approximatives et peuvent varier en fonction des conditions spécifiques et de la pureté de l’échantillon d’acide orthoborique.
Sécurité et dangers de l’acide borique
L’acide orthoborique peut présenter certains risques pour la sécurité s’il est mal manipulé ou mal utilisé. Il est important de prendre les précautions nécessaires. Évitez tout contact direct avec la peau, les yeux et les vêtements, car cela pourrait provoquer une irritation. L’ingestion de grandes quantités peut être toxique et entraîner des problèmes de santé. Lorsque vous travaillez avec de l’acide orthoborique, assurer une bonne ventilation pour éviter l’inhalation de ses poussières ou vapeurs. En cas d’ingestion ou d’exposition accidentelle, consulter immédiatement un médecin. Conservez l’acide orthoborique dans un endroit sûr, hors de portée des enfants et des animaux domestiques. Suivez les procédures d’élimination appropriées pour minimiser l’impact sur l’environnement. Le respect des consignes de sécurité favorise une manipulation sûre et minimise les risques potentiels associés à l’acide orthoborique.
| Symboles de danger | Xn (nocif) |
| Description de la sécurité | Eviter le contact avec la peau et les yeux. Utiliser avec une ventilation adéquate. Consulter un médecin en cas d’ingestion ou d’exposition. Tenir à l’écart des enfants et des animaux domestiques. Suivez les procédures d’élimination appropriées. |
| Numéros d’identification de l’ONU | UN3077 |
| Code SH | 2810.00.90 |
| Classe de danger | 9 (Substances et objets dangereux divers) |
| Groupe d’emballage | III (Danger mineur) |
| Toxicité | Modérément toxique en cas d’ingestion en grande quantité. Peut provoquer une irritation au contact. |
Méthodes de synthèse de l’acide borique
Il existe plusieurs méthodes pour synthétiser l’acide orthoborique.
Méthode d’acidification du borax : Le borax, également connu sous le nom de borate de sodium, est acidifié pour produire de l’acide orthoborique. Pour obtenir de l’acide orthoborique pur, mélangez une solution de borax avec un acide fort, tel que l’acide chlorhydrique (HCl) ou l’acide sulfurique (H₂SO₄) . L’acide réagit avec le borax, libérant de l’acide orthoborique sous forme de précipité. Filtrer, laver et sécher le précipité pour obtenir de l’acide orthoborique pur.
Dans la méthode d’hydrolyse de l’oxyde de bore, hydrolysez l’oxyde de bore (B₂O₃) en le faisant réagir avec de l’eau (H₂O) dans des conditions contrôlées, généralement à des températures élevées. La réaction entre B₂O₃ et H₂O produit de l’acide orthoborique comme produit principal. Concentrer, cristalliser et sécher la solution d’acide orthoborique résultante pour obtenir de l’acide orthoborique solide.
L’industrie utilise largement les deux méthodes mentionnées ci-dessus pour produire de l’acide orthoborique. Le choix de la méthode dépend de facteurs tels que la disponibilité des matières premières, la pureté souhaitée et l’échelle de production. Il est important de noter que ces méthodes de synthèse impliquent l’utilisation de mesures de sécurité appropriées et le respect des réglementations applicables pour garantir la manipulation et la production sûres d’acide orthoborique.
Utilisations de l’acide borique
L’acide orthoborique trouve de nombreuses applications dans diverses industries en raison de ses propriétés polyvalentes. Voici quelques utilisations courantes de l’acide orthoborique :
- Insecticide et lutte antiparasitaire : L’acide orthoborique contrôle efficacement les parasites comme les fourmis, les cafards et les termites en perturbant leur système digestif, pour finalement les éliminer.
- Conservateur du bois : L’acide orthoborique préserve le bois en le protégeant des attaques de champignons et d’insectes. Les gens traitent généralement le bois pour la construction, les meubles et autres structures en bois.
- Ignifuge : L’acide orthoborique améliore les propriétés ignifuges des matériaux tels que les textiles, les tissus d’ameublement et l’isolation, réduisant ainsi leur inflammabilité et empêchant la propagation du feu.
- Gouttes oculaires et solution pour lentilles de contact : Les fabricants utilisent de l’acide orthoborique dans la production de gouttes oculaires et de solutions pour lentilles de contact pour nettoyer et lubrifier les yeux, soulageant ainsi la sécheresse et les irritations.
- Tampon pH : En raison de sa nature faiblement acide, l’acide orthoborique agit comme un tampon pH dans divers produits. Il aide à maintenir les niveaux de pH souhaités dans les cosmétiques, les produits de soins personnels et les formulations pharmaceutiques.
- Utilisations antiseptiques et médicinales : L’acide orthoborique possède des propriétés antiseptiques, ce qui le rend utile dans le traitement des plaies mineures, des infections cutanées et de certaines affections oculaires. Diverses préparations pharmaceutiques utilisent également de l’acide orthoborique dans leur production.
- Industrie du verre et de la céramique : L’acide orthoborique est un ingrédient essentiel dans la fabrication de verre, de céramique et de fibre de verre résistants à la chaleur. Cela contribue à améliorer la résistance, la durabilité et la résistance à la chaleur de ces matériaux.
Les utilisateurs de l’acide orthoborique incluent un large éventail d’applications, comme en témoignent les exemples mentionnés ci-dessus. Ses diverses propriétés en font un composé précieux dans diverses industries, des produits ménagers aux procédés industriels.
Des questions:
Q : Que se passe-t-il lorsque de l’acide borique est ajouté à l’eau ?
R : Lorsque l’acide orthoborique est ajouté à l’eau, il se dissout et forme une solution d’acide orthoborique.
Q : L’acide borique est-il un acide protique ? Expliquer.
R : Oui, l’acide orthoborique est un acide protique car il peut donner un proton (H+) lors d’une réaction chimique.
Q : Comment préparer l’acide borique ?
R : L’acide orthoborique peut être préparé par acidification du borax (borate de sodium) ou par hydrolyse de l’oxyde de bore (B₂O₃).
Q : Comment dissoudre l’acide borique dans l’eau ?
R : Pour dissoudre l’acide orthoborique dans l’eau, ajoutez-le simplement à l’eau et remuez jusqu’à ce que l’acide orthoborique se dissolve complètement.
Q : Le borax est-il la même chose que l’acide borique ?
R : Non, le borax (borate de sodium) n’est pas la même chose que l’acide orthoborique (H₃BO₃), bien que les deux contiennent du bore.
Q : Qu’est-ce que l’acide borique ?
R : L’acide orthoborique est un composé cristallin blanc doté de propriétés antiseptiques, insecticides et conservatrices, couramment utilisé dans diverses applications.
Q : Où acheter de l’acide borique ?
R : L’acide orthoborique peut être acheté auprès de diverses sources, notamment des détaillants en ligne, des pharmacies et des magasins vendant des produits chimiques ou des produits ménagers.
Q : L’acide borique est-il sans danger pour les humains ?
R : L’acide orthoborique peut être toxique s’il est ingéré en grande quantité, mais lorsqu’il est utilisé selon les instructions et en quantités appropriées, il est généralement considéré comme sans danger pour les humains.
Q : Quelles substances sont des bases ? Cochez tout ce qui s’applique : NaOH, KOH, H₃BO₃, NaCl, Ca(OH)₂, Fe₂O₃.
R : Les bases parmi les substances données sont NaOH, KOH, Ca(OH)₂.
Q : Quelle formule représente l’acide borique ? H₃B, H₃BO₃, HBr, H₃PO₄.
R : La formule qui représente l’acide orthoborique est H₃BO₃.
Q : Quel est le nombre d’oxydation du bore (B) dans H₃BO₃ ?
R : Le nombre d’oxydation du bore (B) dans H₃BO₃ est de +3.
Q : H₃BO₃ est-il un acide fort ?
R : Non, H₃BO₃ (acide orthoborique) est un acide faible.
Q : H₃BO₃ est-il un électrolyte fort ou faible ?
R : H₃BO₃ (acide orthoborique) est un électrolyte faible.
