L’acétone ou diméthylcétone est un solvant incolore et inflammable avec une odeur distincte et piquante. Il est utilisé dans la production de plastiques, de fibres et d’autres produits chimiques, ainsi que pour le nettoyage et le dégraissage. On le trouve également dans le dissolvant pour vernis à ongles.
| Nom UICPA | Propanone |
| Formule moléculaire | C3H6O |
| Numero CAS | 67-64-1 |
| Synonymes | 2-propanone, diméthylcétone, diméthylformaldéhyde, acide pyroacétique, β-cétopropane |
| InChI | InChI=1S/C3H6O/c1-3(2)4/h3-4H,1-2H3 |
Propriétés de l’acétone
Masse molaire de l’acétone
La masse molaire de l’acétone est de 58,08 g/mol. Cela signifie qu’une mole d’acétone contient 58,08 grammes de substance. La masse molaire est une propriété physique importante car elle est utilisée pour calculer le nombre de moles d’une substance dans un échantillon et pour déterminer la quantité d’une substance nécessaire dans une réaction chimique.
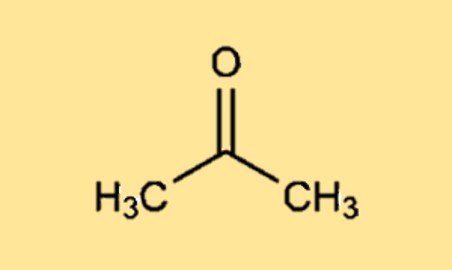
Structure de l’acétone
La diméthylcétone (CH3C(=O)CH3) est une cétone simple à trois carbones avec une formule moléculaire de C3H6O. La molécule a un groupe carbonyle (-C=O) au centre, avec un groupe méthyle (-CH3) de chaque côté du groupe carbonyle.
Point d’ébullition de l’acétone
Le point d’ébullition de l’acétone est de 56,5°C. Cela signifie qu’à 56,5°C, la pression de vapeur de la diméthylcétone est égale à la pression atmosphérique, ce qui fait bouillir le liquide et se transforme en gaz. Le point d’ébullition est une propriété physique importante car il est utilisé pour déterminer la pureté d’une substance et les conditions dans lesquelles une substance peut être distillée ou évaporée.
Point de fusion de l’acétone
Le point de fusion de l’acétone est de -94°C. Cela signifie qu’à -94°C, la diméthylcétone solide commencera à se transformer en liquide. Le point de fusion est une propriété physique importante car il est utilisé pour déterminer la pureté d’une substance et les conditions dans lesquelles une substance peut être solidifiée.
Densité de l’acétone g/ml
La densité de l’acétone est de 0,7893 g/ml. Cela signifie qu’un millilitre de diméthylcétone pèse 0,7893 gramme. La densité est une propriété physique importante car elle est utilisée pour déterminer la quantité d’une substance dans un volume donné.
Poids moléculaire de l’acétone
Le poids moléculaire de l’acétone est de 58,08 g/mol. Cela signifie qu’une mole de molécules de diméthylcétone pèse 58,08 grammes. Le poids moléculaire est une propriété physique importante car il est utilisé pour déterminer le nombre de moles d’une substance dans un échantillon et pour calculer la quantité d’une substance nécessaire dans une réaction chimique.
| Apparence | Liquide clair et incolore |
| Gravité spécifique | 0,79 |
| Couleur | Clair, incolore |
| Odeur | Piquant, sucré |
| Masse molaire | 58,08 g/mole |
| Densité | 0,79 g/cm³ |
| Point de fusion | -95,3°C |
| Point d’ébullition | 56,5°C |
| Point d’éclair | -20°C |
| Solubilité dans l’eau | Miscible |
| Solubilité | Soluble dans la plupart des solvants organiques |
| Pression de vapeur | 49,7 kPa à 20°C |
| Densité de vapeur | 2,05 g/L |
| pKa | 19.2 |
| PH | 3,0 (acide) |
Sécurité et dangers de l’acétone
L’acétone est un solvant hautement inflammable avec une forte odeur. Une exposition prolongée à l’acétone peut provoquer une irritation cutanée et des problèmes respiratoires. Il est important de stocker la diméthylcétone dans un endroit bien ventilé, à l’écart des sources de chaleur et des étincelles. Lors de l’utilisation de diméthylcétone, il est important de porter des gants et une protection oculaire appropriée. Ne fumez pas et ne mangez pas lorsque vous utilisez de l’acétone et évitez tout contact avec des flammes nues. En cas d’ingestion, la diméthylcétone peut provoquer des troubles digestifs et doit être immédiatement traitée comme une urgence médicale. Une manipulation et une utilisation appropriées de la diméthylcétone sont cruciales pour garantir la sécurité et prévenir les accidents.
| Symboles de danger | Inflammable |
| Description de la sécurité | La diméthylcétone est hautement inflammable et peut facilement s’enflammer. |
| Numéros d’identification de l’ONU | UN1090 |
| Code SH | 2914.11.00 |
| Classe de danger | 3 |
| Groupe d’emballage | II |
| Toxicité | Légèrement toxique par inhalation, ingestion et contact cutané. |
Méthodes de synthèse de l’acétone
L’acétone est synthétisée à l’aide de deux méthodes principales : le procédé au cumène et le procédé de déshydrogénation. Le processus au cumène implique l’alkylation du benzène avec du propylène pour former du cumène, qui est ensuite oxydé pour former du phénol et de l’acétone. Le processus de déshydrogénation implique la déshydrogénation de l’alcool isopropylique, produisant de la diméthylcétone comme sous-produit. Les deux méthodes sont largement utilisées dans l’industrie et donnent lieu à des rendements élevés en diméthylcétone. Le procédé au cumène est la méthode la plus couramment utilisée pour la production commerciale de diméthylcétone, car elle est rentable et fournit une diméthylcétone de haute pureté. Le processus de déshydrogénation est généralement utilisé pour une production à plus petite échelle et pour des applications nécessitant de la diméthylcétone de haute pureté.
Utilisations de l’acétone
Les gens utilisent largement la diméthylcétone comme solvant pour diverses substances en raison de sa nature incolore et volatile. Dans l’industrie cosmétique et de beauté, il agit comme ingrédient dans les dissolvants pour vernis à ongles, les lotions pour le corps et autres produits de soin de la peau. La fabrication de produits pharmaceutiques, d’adhésifs et de résines nécessite également de l’acétone. Il nettoie efficacement les composants électroniques, dégraisse les moteurs et élimine les résidus de colle. Les scientifiques l’utilisent comme solvant pour diverses réactions chimiques en laboratoire. De plus, il améliore les performances du moteur en tant qu’additif pour carburant en raison de son faible point d’ébullition. Son évaporation facile sans laisser de résidus en fait un choix idéal pour de nombreuses applications.
