L’acétaldéhyde est un composé organique volatil produit lors du métabolisme de l’alcool, provoquant des symptômes de gueule de bois. Il est également utilisé comme intermédiaire chimique dans diverses industries.
| Nom UICPA | Éthanal |
| Formule moléculaire | C₂H₄O |
| Numero CAS | 75-07-0 |
| Synonymes | Aldéhyde d’éthyle, aldéhyde acétique, éthanal, 1-oxapropylène |
| InChI | InChI=1S/C2H4O/c1-2-3/h2H,1H3 |
Propriétés de l’acétaldéhyde
Formule acétaldéhyde
La formule de l’éthanal est C₂H₄O. Il se compose de deux atomes de carbone, de quatre atomes d’hydrogène et d’un atome d’oxygène. La formule représente le rapport des atomes présents dans une molécule d’éthanal.
Acétaldéhyde Masse molaire
La masse molaire de l’éthanal est d’environ 44,05 g/mol. Il est calculé en additionnant les masses atomiques de tous les atomes de la molécule selon la formule C₂H₄O.
Point d’ébullition de l’acétaldéhyde
L’éthanal a un point d’ébullition d’environ 20,2 degrés Celsius (68,4 degrés Fahrenheit). Il s’agit de la température à laquelle l’éthanal passe de l’état liquide à l’état gazeux sous pression atmosphérique standard.
Acétaldéhyde Point de fusion
Le point de fusion de l’éthanal est d’environ -123,5 degrés Celsius (-190,3 degrés Fahrenheit). C’est la température à laquelle l’éthanal passe de l’état solide à l’état liquide.
Acétaldéhyde Densité g/mL
La densité de l’éthanal est d’environ 0,78 g/mL. Cette valeur représente la masse d’éthanal par unité de volume. Il indique à quel point les molécules sont serrées dans un volume donné de la substance.
Acétaldéhyde Poids moléculaire
Le poids moléculaire de l’éthanal est d’environ 44,05 g/mol. C’est la somme des poids atomiques de tous les atomes de la molécule et s’exprime en grammes par mole.
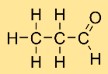
Structure de l’acétaldéhyde
L’éthanal a une structure linéaire, avec des atomes de carbone liés les uns aux autres et à l’atome d’oxygène. La molécule possède un atome de carbone central, deux atomes d’hydrogène qui lui sont attachés et un atome d’oxygène lié à l’atome de carbone.
Solubilité de l’acétaldéhyde
L’éthanal est soluble dans l’eau et dans les solvants organiques. Il se dissout facilement dans l’eau en raison de la présence de groupes fonctionnels polaires. La solubilité de l’éthanal dans l’eau diminue avec l’augmentation de la température.
| Apparence | Liquide incolore |
| Gravité spécifique | 0,780 g/ml |
| Couleur | Incolore |
| Odeur | Piquant, fruité |
| Masse molaire | 44,05 g/mole |
| Densité | 0,78 g/ml |
| Point de fusion | -123,5 °C |
| Point d’ébullition | 20,2 °C |
| Point d’éclair | -36 °C |
| Solubilité dans l’eau | Miscible |
| Solubilité | Soluble dans les solvants organiques tels que l’éther, l’alcool, l’acide acétique |
| La pression de vapeur | 97,2 mmHg à 25 °C |
| Densité de vapeur | 1,52 (air = 1) |
| pKa | 13h55 |
| pH | 3,5-4,5 |
Sécurité et dangers de l’acétaldéhyde
L’éthanal pose plusieurs problèmes de sécurité et de danger. Il est hautement inflammable, des précautions doivent donc être prises pour éviter les sources d’inflammation. L’inhalation de vapeurs d’éthanal peut irriter le système respiratoire, les yeux et la peau. Une exposition prolongée peut entraîner des effets plus graves sur la santé. L’éthanal est également un cancérigène potentiel, associé à un risque accru de cancer. Une ventilation adéquate et un équipement de protection individuelle doivent être utilisés lors de la manipulation de l’éthanal. De plus, il est important de stocker et de manipuler l’éthanal dans un endroit bien ventilé, à l’écart des substances incompatibles. Le respect des directives et protocoles de sécurité est crucial pour minimiser les risques associés à l’éthanal.
| Symboles de danger | Inflammable, nocif, cancérigène |
| Description de la sécurité | Tenir à l’écart de la chaleur, des étincelles et des flammes nues. Évitez l’inhalation et le contact avec les yeux et la peau. Utilisez une ventilation adéquate et un équipement de protection individuelle. Conserver dans un endroit frais et bien ventilé, à l’écart des substances incompatibles. Suivez les consignes et les protocoles de sécurité. |
| Numéros d’identification de l’ONU | UN1089 |
| Code SH | 29121900 |
| Classe de danger | 3 (Liquides inflammables) |
| Groupe d’emballage | II |
| Toxicité | Toxicité aiguë : nocif en cas d’ingestion, d’inhalation ou d’absorption cutanée. Une exposition à long terme peut augmenter le risque de cancer. |
Méthodes de synthèse de l’acétaldéhyde
Il existe plusieurs méthodes pour synthétiser l’éthanal. Une approche courante consiste à oxyder l’éthanol à l’aide d’agents oxydants comme le dichromate de potassium ou l’oxyde de cuivre dans des conditions acides. Cette réaction produit de l’éthanal comme produit principal.
Une autre méthode consiste à déshydrogéner l’éthylène en le faisant passer sur un catalyseur tel que l’argent ou le cuivre à haute température. Ce processus élimine les atomes d’hydrogène de l’éthylène , entraînant la formation d’éthanal.
Dans l’hydratation de l’acétylène , on peut obtenir de l’éthanal. Lorsque l’acétylène gazeux réagit avec l’eau en présence de catalyseurs comme le sulfate mercurique ou l’acide phosphorique, il produit de l’éthanal.
Des agents oxydants appropriés comme l’acide nitrique ou le permanganate de potassium peuvent être utilisés pour produire de l’éthanal en oxydant l’éthylène glycol. Cette oxydation convertit l’éthylène glycol en éthanal.
Ces exemples illustrent diverses méthodes de synthèse de l’éthanal, chacune avec ses propres avantages. Le choix de la méthode peut dépendre de facteurs tels que la disponibilité des matières premières, le rendement souhaité et les conditions de réaction.
Utilisations de l’acétaldéhyde
L’éthanal a diverses utilisations dans différentes industries. Voici quelques-unes de ses principales applications :
- Intermédiaire chimique : L’éthanal sert d’intermédiaire chimique important dans la production de nombreux composés organiques, notamment l’acide acétique, la pyridine et le pentaérythritol.
- Industrie alimentaire et des boissons : Dans l’industrie alimentaire et des boissons, l’éthanal sert d’agent aromatisant et de conservateur. L’éthanal confère des saveurs fruitées ou de noisette à divers produits, tels que les jus de fruits, les bonbons et les produits de boulangerie.
- Production de plastique et de résine : les fabricants utilisent l’éthanal pour produire des plastiques et des résines, notamment de l’acétate de polyvinyle (PVA) et du polyacétal.
Ces matériaux trouvent des applications dans les adhésifs, les revêtements et les fibres synthétiques. - Produits pharmaceutiques : L’éthanal est un précurseur dans la synthèse de nombreux composés pharmaceutiques. L’éthanal joue un rôle dans la fabrication de vitamines, d’antipaludiques et de sédatifs.
- Industrie du caoutchouc : La production de caoutchouc synthétique implique l’utilisation d’éthanal. Il facilite la réticulation des polymères de caoutchouc, améliorant ainsi leur durabilité et leur élasticité.
- Industrie textile : L’éthanal trouve une application comme agent de teinture et de finition dans l’industrie textile. Il contribue à améliorer la solidité des couleurs et la qualité globale des matières textiles.
- Carburant et énergie : L’éthanal est un candidat potentiel pour les biocarburants en raison de sa teneur élevée en énergie. L’éthanal fermente activement pour se transformer en éthanol ou sert activement d’additif pour carburant.
Ce ne sont là que quelques exemples des utilisations polyvalentes de l’éthanal. Ses diverses propriétés en font un composant précieux dans divers processus industriels, contribuant au développement d’une large gamme de produits dans de multiples secteurs.
Des questions:
Q : Comment éliminer l’acétaldéhyde du corps ?
R : L’éthanal est naturellement décomposé par les enzymes du foie, mais le maintien d’un mode de vie sain, comprenant une bonne hydratation et une alimentation équilibrée, peut soutenir les processus de détoxification du corps.
Q : Qu’est-ce que l’acétaldéhyde ?
R : L’éthanal est un composé organique volatil qui est naturellement produit dans le corps lors du métabolisme de l’alcool et que l’on retrouve également dans divers processus industriels et produits alimentaires.
Q : Quelles orbitales atomiques ou hybrides constituent la liaison entre C2 et O dans l’acétaldéhyde, CH3CHO ?
R : La liaison entre C2 et O dans l’acétaldéhyde est formée par le chevauchement de l’orbitale hybride sp² du carbone et de l’orbitale hybride sp² de l’oxygène.
Q : Comment l’acétaldéhyde affecte-t-il le foie ?
R : L’éthanal peut causer des dommages au foie en interférant avec ses fonctions normales, entraînant une inflammation, un stress oxydatif et une accumulation de graisse dans le foie.
Q : Quelle est l’odeur de l’acétaldéhyde ?
R : L’éthanal a une odeur piquante et fruitée, souvent décrite comme étant semblable à celle des pommes fraîchement coupées ou du dissolvant pour vernis à ongles.
Q : L’acétaldéhyde est-il soluble dans l’eau ?
R : Oui, l’éthanal est soluble dans l’eau. Il se dissout facilement en raison de la présence de groupes fonctionnels polaires.
Q : Dois-je éviter de manger des aliments contenant de l’acétaldéhyde ?
R : L’éthanal est naturellement présent dans de nombreux aliments, notamment les fruits, les légumes et les produits fermentés. Une consommation modérée de ces aliments est généralement sans danger pour la plupart des individus.
Q : Dans quoi trouve-t-on l’acétaldéhyde ?
R : L’éthanal peut être trouvé dans les boissons alcoolisées, les fruits, les légumes, le café, le pain et divers produits alimentaires fermentés.
Q : Quel est le goût de l’acétaldéhyde ?
R : L’éthanal a un goût piquant et amer.
Q : Comment conserver l’acétaldéhyde ?
R : L’éthanal doit être stocké dans un endroit frais et bien ventilé, à l’écart des sources d’inflammation, des substances incompatibles et de la lumière directe du soleil. Il est généralement stocké dans des conteneurs scellés.
Q : Comment l’acétaldéhyde affecte-t-il le corps ?
R : L’éthanal peut avoir des effets toxiques sur le corps, provoquant des symptômes tels que des maux de tête, des nausées et des bouffées vasomotrices, en particulier lorsqu’il est produit en grande quantité au cours du métabolisme de l’alcool.
Q : À quoi sert l’acétaldéhyde ?
R : L’éthanal est utilisé comme intermédiaire chimique dans diverses industries, notamment l’alimentation et les boissons, les produits pharmaceutiques, les plastiques et les textiles.
Q : Comment prononcer l’acétaldéhyde ?
R : Euh-voir-tuhl-deh-hahyd.
