Le nitrate de sodium (NaNO3) est un composé couramment utilisé dans l’industrie alimentaire comme conservateur. Il est également utilisé dans les engrais et les explosifs en raison de ses propriétés oxydantes.
| Nom UICPA | Nitrate de sodium |
| Formule moléculaire | NaNO3 |
| Numero CAS | 7631-99-4 |
| Synonymes | Salpêtre du Chili, Niter cubique, Salpêtre de sodium |
| InChI | InChI=1S/NO3.Na/c2-1(3)4;/q-1;+1 |
Propriétés du nitrate de sodium
Formule de nitrate de sodium
La formule chimique du nitrate de sodium est NaNO3. La formule représente le nombre et les types d’atomes qui composent une molécule de nitrate de sodium. Cela indique que chaque molécule de nitrate de sodium contient un atome de sodium, un atome d’azote et trois atomes d’oxygène. La formule est importante pour comprendre les propriétés chimiques du nitrate de sodium et pour son utilisation dans diverses applications.
Nitrate De Sodium Masse molaire
NaNO3 a une masse molaire de 84,9947 g/mol. La masse molaire est la masse d’une mole d’une substance et est calculée en additionnant les masses atomiques de tous les atomes d’une molécule. NaNO3 contient un atome de Na, un atome de N et trois atomes d’O. Les masses atomiques de ces atomes sont de 22,98977 g/mol pour le sodium, 14,00674 g/mol pour l’azote et 15,9994 g/mol pour l’oxygène. Par conséquent, la masse molaire de NaNO3 est calculée comme suit :
Masse molaire = (1 x 22,98977) + (1 x 14,00674) + (3 x 15,9994) = 84,9947 g/mol
Point d’ébullition du nitrate de sodium
Le point d’ébullition du NaNO3 est de 380 °C (716 °F). Le point d’ébullition est la température à laquelle une substance passe d’un liquide à un gaz à pression atmosphérique. NaNO3 est un composé ionique doté de fortes forces intermoléculaires qui maintiennent ses particules ensemble. Ces forces intermoléculaires nécessitent une grande quantité d’énergie pour être brisées, c’est pourquoi le point d’ébullition du NaNO3 est relativement élevé.
Point de fusion du nitrate de sodium
NaNO3 a un point de fusion de 308 °C (586 °F). Le point de fusion est la température à laquelle une substance passe d’un solide à un liquide à pression atmosphérique. NaNO3 est un composé ionique qui possède une structure cristalline avec de fortes liaisons ioniques entre ses particules. Ces liaisons nécessitent une grande quantité d’énergie pour être rompues, c’est pourquoi le point de fusion du NaNO3 est relativement élevé.
Densité du nitrate de sodium g/mL
La densité de NaNO3 est de 2,257 g/mL. La densité est la masse par unité de volume d’une substance. NaNO3 est un solide cristallin blanc avec une densité relativement élevée en raison de ses particules étroitement tassées. Il est important de noter que la densité du NaNO3 peut varier en fonction de facteurs tels que la température et la pression.
Nitrate De Sodium Poids moléculaire
Le poids moléculaire de NaNO3 est de 84,9947 g/mol. Le poids moléculaire est la somme des poids atomiques de tous les atomes d’une molécule. Comme mentionné précédemment, NaNO3 contient un atome de sodium, un atome d’azote et trois atomes d’oxygène, qui contribuent à son poids moléculaire.
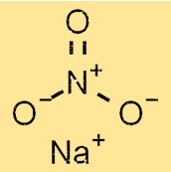
Structure du nitrate de sodium
NaNO3 a une structure cristalline composée d’ions Na+ et NO3-. Les cations Na+ et les anions NO3- sont disposés dans une structure en réseau maintenus ensemble par de fortes liaisons ioniques. La structure du NaNO3 est importante pour comprendre ses propriétés physiques et chimiques.
| Apparence | Cristaux ou poudre blancs |
| Gravité spécifique | 2,257 g/cm3 à 20°C |
| Couleur | Incolore |
| Odeur | Inodore |
| Masse molaire | 84,9947 g/mole |
| Densité | 2,257 g/cm3 à 20°C |
| Point de fusion | 308 °C (586 °F) |
| Point d’ébullition | 380 °C (716 °F) |
| Point d’éclair | N’est pas applicable |
| Solubilité dans l’eau | 87 g/100 ml (20 °C) |
| Solubilité | Soluble dans le glycérol, l’ammoniac et le peroxyde d’hydrogène. Insoluble dans l’alcool. |
| Pression de vapeur | 0,003 mm Hg à 20 °C |
| Densité de vapeur | N’est pas applicable |
| pKa | -1,4 |
| pH | 7 (solution à 10 % dans l’eau) |
Sécurité et dangers du nitrate de sodium
NaNO3 peut présenter plusieurs dangers pour la santé humaine et l’environnement. C’est un léger irritant et peut provoquer une irritation de la peau et des yeux au contact. L’inhalation de poussières de NaNO3 peut également provoquer une irritation respiratoire. NaNO3 peut réagir avec des matériaux combustibles et provoquer un incendie ou une explosion. Il est également toxique pour la vie aquatique et ne doit pas être rejeté dans les cours d’eau. NaNO3 doit être manipulé avec précaution et un équipement de protection approprié doit être porté lors de sa manipulation. Il doit être stocké dans un endroit sec et bien ventilé, à l’écart des matériaux incompatibles. Des méthodes d’élimination appropriées doivent également être suivies pour éviter la contamination de l’environnement.
| Symboles de danger | Ô, Xi |
| Description de la sécurité | Évitez tout contact avec des matériaux combustibles, portez un équipement de protection et stockez dans un endroit sec et bien ventilé. Éliminer correctement. |
| Numéros d’identification de l’ONU | UN1498 (anhydre) / UN1499 (fondu) |
| Code SH | 28342910 |
| Classe de danger | 5.1 (Agent comburant) |
| Groupe d’emballage | III |
| Toxicité | DL50 (orale, rat) : 1260 mg/kg |
Méthodes de synthèse du nitrate de sodium
Plusieurs méthodes peuvent synthétiser NaNO3, notamment la réaction de l’acide nitrique avec de l’hydroxyde de sodium ou la réaction de l’acide nitrique avec du carbonate de sodium .
La première méthode consiste à ajouter progressivement une solution d’ hydroxyde de sodium à une solution d’ acide nitrique sous agitation jusqu’à ce que le pH atteigne 7-8. La solution réagit pour former du NaNO3, qu’une personne peut évaporer et cristalliser pour obtenir le composé solide.
Une autre méthode implique la réaction du carbonate de sodium avec l’acide nitrique . La personne ajoute du carbonate de sodium à l’acide nitrique jusqu’à ce que l’effervescence cesse, puis chauffe le mélange jusqu’à ce que le dégagement de dioxyde de carbone cesse. Ils s’évaporent ensuite et cristallisent la solution obtenue pour obtenir NaNO3.
La production de NaNO3 peut aboutir à son obtention comme sous-produit par la production d’ acide nitrique ou par oxydation de l’ammoniac avec un catalyseur au platine.
Utilisations du nitrate de sodium
NaNO3 a un large éventail d’applications industrielles, agricoles et médicales en raison de ses propriétés chimiques et physiques. Certaines des utilisations de NaNO3 incluent :
- Engrais : Couramment utilisé comme engrais azoté en agriculture en raison de sa haute solubilité et de ses propriétés de libération rapide.
- Conservateur alimentaire : utilisé comme conservateur alimentaire pour empêcher la croissance de bactéries et de champignons dans les viandes transformées telles que le jambon, le bacon et les hot-dogs.
- Production de verre : utilisé comme fondant dans la production de verre pour abaisser son point de fusion et améliorer sa clarté.
- Pyrotechnie : Ingrédient clé dans la production de feux d’artifice et autres dispositifs pyrotechniques en raison de ses propriétés oxydantes.
- Fluide caloporteur : utilisé comme fluide caloporteur dans les centrales solaires pour stocker et transférer l’énergie thermique.
- Applications médicales : Utilisé dans le traitement de l’angine de poitrine, une maladie cardiaque qui provoque des douleurs thoraciques en raison d’un flux sanguin insuffisant vers le cœur.
- Applications industrielles : également utilisé dans la production de colorants, d’agents de blanchiment et d’autres produits chimiques.
Questions :
Q : Le nitrate de sodium est-il soluble dans l’eau ?
R : Oui, NaNO3 est hautement soluble dans l’eau, avec une solubilité de 91 grammes pour 100 millilitres d’eau à température ambiante.
Q : À quoi sert le nitrate de sodium ?
R : NaNO3 est utilisé à diverses fins, notamment comme engrais, conservateur alimentaire, flux de production de verre, oxydant pyrotechnique, fluide caloporteur et dans des applications médicales et industrielles.
Q : Le nitrate de sodium est-il un électrolyte puissant ?
R : Oui, NaNO3 est un électrolyte puissant, ce qui signifie qu’il se dissocie complètement en ions lorsqu’il est dissous dans l’eau, permettant ainsi la conduction de l’électricité.
Q : Le NaNO3 est-il soluble dans l’eau ?
R : Oui, NaNO3 est hautement soluble dans l’eau, avec une solubilité de 91 grammes pour 100 millilitres d’eau à température ambiante.
Q : Le NaNO3 est-il soluble ?
R : Oui, NaNO3 est soluble dans l’eau, mais il est insoluble dans certains solvants organiques tels que l’éthanol et l’éther.
Q : Quel sel est produit lorsque NH4OH réagit avec HNO3 ? KNO2, NaNO3, NH4NO3 ou NH4NO2 ?
R : Le sel produit lorsque NH4OH réagit avec HNO3 est NH4NO3, également connu sous le nom de nitrate d’ammonium.
Q : NaNO3 est-il un acide ou une base ?
R : NaNO3 est un composé neutre et ni un acide ni une base.
Q : Qu’est-ce que NaNO3 ?
R : NaNO3 est la formule chimique du nitrate de sodium, qui est un solide cristallin blanc ayant diverses applications industrielles, agricoles et médicales.
