Le diéthylène glycol (DEG) est un composé chimique couramment utilisé comme solvant, antigel et dans la fabrication de résines et de plastiques. Il peut être toxique s’il est ingéré ou inhalé, c’est pourquoi une manipulation et un stockage appropriés sont importants.
| Nom UICPA | éthane-1,2-diol |
| Formule moléculaire | C4H10O2 |
| Numero CAS | 111-46-6 |
| Synonymes | DEG, 2,2′-oxybiséthanol, diglycol, 2-hydroxyéthyléther, 1,2-dihydroxyéthane |
| InChI | InChI=1S/C4H10O2/c5-3-1-2-4-6/h5-6H,1-4H2 |
Propriétés du diéthylèneglycol
Diéthylène Glycol FDS
Selon la fiche signalétique, le DEG est considéré comme une substance dangereuse pouvant avoir des effets graves sur la santé en cas d’ingestion ou d’inhalation. C’est également un liquide inflammable qui peut s’enflammer s’il est exposé à la chaleur ou à une flamme nue. La fiche signalétique fournit des conseils sur la façon de manipuler, de stocker et de transporter le DEG en toute sécurité, ainsi que sur les procédures de premiers secours en cas d’exposition accidentelle. Il est important de lire attentivement et de comprendre la fiche signalétique avant de travailler avec DEG pour assurer votre sécurité et celle des autres.
Formule de diéthylèneglycol
La formule chimique du diéthylèneglycol est C4H10O2. Cette formule représente la disposition des atomes dans le DEG, y compris ses éléments constitutifs (carbone, hydrogène et oxygène) ainsi que le nombre et le type de liaisons entre eux. La formule du DEG est importante pour comprendre ses propriétés chimiques et son comportement dans les réactions.
Diéthylène Glycol Masse molaire
Le DEG a une masse molaire de 106,12 g/mol. Cette valeur est calculée en additionnant les masses atomiques de ses éléments constitutifs : deux atomes de carbone, quatre atomes d’hydrogène et deux atomes d’oxygène. La masse molaire du DEG est importante pour déterminer ses propriétés physiques et chimiques, notamment ses points d’ébullition et de fusion.
Point d’ébullition du diéthylèneglycol
Le point d’ébullition du DEG est de 245°C (473°F). Ceci est relativement élevé par rapport à d’autres solvants courants, tels que l’éthanol et l’acétone, en raison de son poids moléculaire élevé et de ses fortes forces intermoléculaires. Le point d’ébullition du DEG est un facteur important dans son utilisation comme fluide caloporteur et antigel.
Diéthylène Glycol Point de fusion
Le point de fusion du DEG est de -10°C (14°F). Cette valeur relativement faible est due à la présence de groupes hydroxyles polaires dans sa structure, qui favorisent les liaisons intermoléculaires entre les molécules. Le point de fusion du DEG est important pour déterminer son comportement en tant que solvant et son aptitude à être utilisé dans des applications à basse température.
Densité du diéthylèneglycol g/mL
La densité du DEG est de 1,118 g/mL à 25°C (77°F). Cette valeur est supérieure à celle de l’eau, qui a une densité de 1 g/mL, en raison du poids moléculaire élevé et des fortes forces intermoléculaires du DEG. La densité du DEG est un facteur important dans son utilisation comme solvant, ainsi que pour déterminer son comportement dans des mélanges avec d’autres liquides.
Diéthylène Glycol Poids moléculaire
Le poids moléculaire du DEG est de 106,12 g/mol. Cette valeur est importante pour déterminer les propriétés physiques et chimiques du DEG, ainsi que son comportement dans les réactions chimiques. Le poids moléculaire du DEG est également important pour déterminer sa concentration dans les solutions et les mélanges.
Structure du diéthylèneglycol
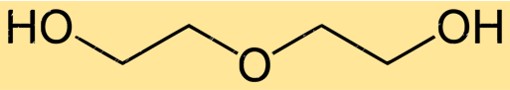
La structure du diéthylèneglycol se compose de deux groupes hydroxyle (-OH) attachés à un squelette central éthylène (-CH2CH2-). Cette structure favorise une forte liaison intermoléculaire entre les molécules, conférant au DEG ses points d’ébullition et de fusion élevés. La structure du DEG est importante pour déterminer son comportement en tant que solvant, ainsi que son aptitude à être utilisée dans diverses applications.
| Apparence | Liquide clair et incolore |
| Gravité spécifique | 1,118 g/mL à 25°C |
| Couleur | Incolore |
| Odeur | Inodore |
| Masse molaire | 106,12 g/mole |
| Densité | 1,118 g/mL à 25°C |
| Point de fusion | -10°C (14°F) |
| Point d’ébullition | 245°C (473°F) |
| Point d’éclair | 138°C (280°F) |
| Solubilité dans l’eau | Complètement soluble |
| Solubilité | Miscible avec de nombreux solvants organiques |
| Pression de vapeur | 0,0005 mmHg à 20°C |
| Densité de vapeur | 3,6 (air = 1) |
| pKa | 14h00 |
| pH | Neutre (pH 7) |
Sécurité et dangers du diéthylèneglycol
Le diéthylène glycol (DEG) est une substance dangereuse qui peut avoir de graves effets sur la santé si elle n’est pas manipulée correctement. L’exposition au DEG peut se produire par inhalation, ingestion ou contact cutané. Les symptômes d’exposition peuvent inclure des nausées, des vomissements, des douleurs abdominales, de la diarrhée et une insuffisance rénale. Le DEG est également inflammable et peut former des mélanges explosifs avec l’air. Il est important d’utiliser un équipement de protection approprié, tel que des gants et des respirateurs, lorsque vous travaillez avec du DEG. Les déversements doivent être nettoyés immédiatement et les déchets doivent être éliminés conformément aux réglementations locales. Le DEG doit être stocké dans un endroit frais, sec et bien ventilé, loin des sources de chaleur et des matériaux incompatibles.
| Symboles de danger | Xn (nocif) |
| Description de la sécurité | Eviter le contact avec la peau et les yeux. Ne pas inhaler. Tenir à l’écart des sources d’ignition. Utiliser avec une ventilation adéquate. |
| Numéros d’identification de l’ONU | UN3082, UN1993 |
| Code SH | 2909.44.0000 |
| Classe de danger | 9 (Marchandises dangereuses diverses) |
| Groupe d’emballage | III |
| Toxicité | Toxique par ingestion, inhalation et absorption cutanée. |
Méthodes de synthèse du diéthylèneglycol
Il existe plusieurs méthodes de synthèse du diéthylène glycol (DEG).
Une méthode courante consiste à faire réagir l’oxyde d’éthylène avec l’éthylène glycol en présence d’un catalyseur, tel que l’hydroxyde de sodium ou l’hydroxyde de potassium. Ce procédé produit un mélange de DEG et de triéthylène glycol (TEG), qui peut être séparé par distillation.
Une autre méthode implique la réaction de l’éthylène glycol avec l’acétaldéhyde en présence d’un catalyseur, tel que le zinc ou l’aluminium. Ce processus produit du DEG et de l’eau comme sous-produits. On peut conduire la réaction dans des conditions de reflux et distiller le mélange résultant pour purification.
Une troisième méthode implique la réaction de l’oxyde d’éthylène avec l’éther monométhylique du diéthylèneglycol (DGME) en présence d’un catalyseur, tel que l’hydroxyde de potassium ou l’acide sulfurique. Ce processus produit du DEG et du monoéthylène glycol (MEG) comme sous-produits. Le mélange résultant peut subir une purification par distillation tout en conduisant la réaction dans des conditions de reflux.
Utilisations du diéthylèneglycol
Le diéthylène glycol (DEG) est une substance polyvalente qui est utilisée dans diverses industries en raison de ses propriétés uniques. Certaines utilisations courantes du DEG incluent :
- Solvant industriel : Couramment utilisé comme solvant dans la production de résines, de colorants et d’encres.
- Intermédiaire chimique : utilisé comme élément de base dans la synthèse de divers produits chimiques, notamment des plastifiants, des lubrifiants et des tensioactifs.
- Antigel : Utilisé comme agent antigel dans les systèmes de chauffage et de refroidissement, car son point de congélation est inférieur à celui de l’eau.
- Humectant : Utilisé comme humectant dans la production de textiles et de papier, car il aide à maintenir la teneur en humidité.
- Produits de soins personnels : Utilisés comme ingrédient dans divers produits de soins personnels, tels que le dentifrice, les produits de soins capillaires et les déodorants.
- Pharmaceutique : Utilisé comme solvant dans la production de divers produits pharmaceutiques, notamment des sirops contre la toux et des élixirs.
- Déshydratation du gaz : utilisée pour éliminer l’eau du gaz naturel et d’autres gaz d’hydrocarbures.
- Industrie alimentaire : utilisé comme solvant pour les colorants alimentaires et les arômes.
Des questions:
Q : Comment le diéthylèneglycol est-il synthétisé ?
R : Le DEG est généralement synthétisé par la réaction de l’oxyde d’éthylène avec l’éthylène glycol en présence d’un catalyseur, tel que l’hydroxyde de sodium ou l’hydroxyde de potassium. Une autre méthode implique la réaction de l’éthylène glycol avec l’acétaldéhyde en présence d’un catalyseur, tel que le zinc ou l’aluminium.
Q : Qu’est-ce que le diéthylèneglycol ?
R : Le DEG est un liquide incolore, inodore et hygroscopique qui est couramment utilisé comme solvant, intermédiaire chimique et agent antigel. C’est un type de glycol qui possède deux groupes hydroxyéthyle dans sa molécule.
Q : Le diéthylèneglycol peut-il également être utilisé pour fabriquer des méthamphétamines ?
R : Bien que le DEG ne soit pas couramment utilisé pour fabriquer des méthamphétamines, il est possible qu’il soit utilisé comme solvant ou précurseur dans le processus de fabrication. Cependant, l’utilisation du DEG dans ce contexte serait hautement illégale et dangereuse.
Q : Quelle est la différence entre le diéthylèneglycol et la paraffine ?
R : Le DEG et la paraffine sont deux substances différentes ayant des propriétés chimiques et physiques distinctes. Le DEG est un composé glycolique liquide couramment utilisé comme solvant et intermédiaire chimique, tandis que la paraffine est un hydrocarbure solide cireux couramment utilisé dans les bougies, les cosmétiques et d’autres applications.
Q : Le diéthylèneglycol est-il un fluide newtonien ?
R : Oui, le DEG est considéré comme un fluide newtonien, ce qui signifie que sa viscosité reste constante quel que soit le taux de cisaillement ou la force appliquée. Cette propriété le rend utile dans diverses applications où un débit de fluide constant est important.
