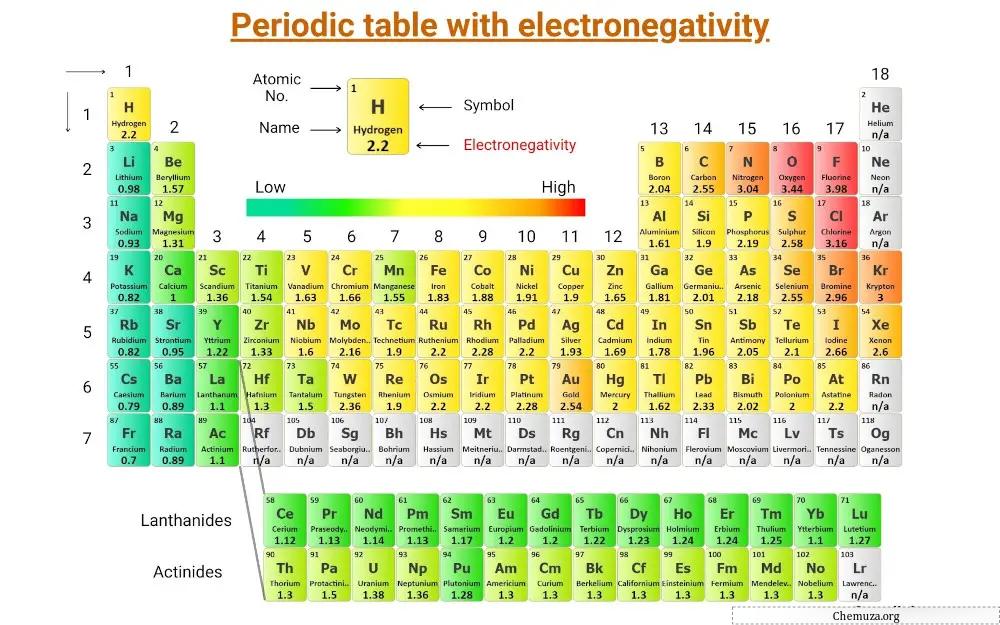
Il s’agit d’un tableau périodique sur lequel est inscrite l’électronégativité des éléments.
(Remarque : l’électronégativité n’a pas d’unité. Linus Pauling était un scientifique qui a conçu une échelle d’électronégativité qui classe les éléments les uns par rapport aux autres. Et cette échelle est connue sous le nom d’échelle d’électronégativité de Pauling.) [1]
Si vous ne savez pas ce qu’est l’électronégativité, voici une brève explication à ce sujet.
Qu’est-ce que l’électronégativité ?
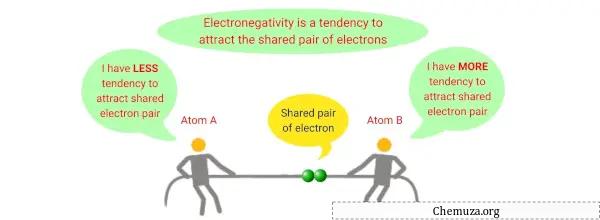
L’électronégativité est une propriété chimique qui décrit la capacité d’un atome à attirer des électrons vers lui lorsqu’il fait partie d’un composé ou d’une molécule.
C’est une mesure de l’attraction relative qu’un atome exerce sur les électrons partagés dans une liaison covalente .
Pourquoi l’électronégativité est-elle importante ?
L’électronégativité joue un rôle crucial dans la prédiction de la nature de la liaison chimique, de la réactivité et des propriétés physiques des molécules .
Cela aide à expliquer pourquoi certains éléments ont tendance à former des types spécifiques de liaisons, telles que des liaisons covalentes ou ioniques, et comment ces liaisons affectent le comportement du composé résultant.
L’électronégativité aide également à prédire la polarité d’une molécule et ses interactions avec d’autres molécules, ce qui est important dans de nombreux domaines, notamment la chimie, la biologie et la science des matériaux.
Que signifie une électronégativité plus élevée ?
Lorsqu’un atome a une électronégativité plus élevée, cela signifie qu’il a une plus grande capacité à attirer des électrons vers lui lorsqu’il fait partie d’un composé chimique ou d’une molécule.
Cela conduit à la formation de liaisons covalentes polaires, où les électrons ne sont pas partagés également entre les atomes.
L’atome ayant l’électronégativité la plus élevée attire les électrons plus près de lui, ce qui entraîne une charge partielle négative, tandis que l’autre atome de la liaison a une charge partielle positive.
Cette polarité affecte les propriétés physiques et chimiques du composé, telles que ses points d’ébullition et de fusion, sa solubilité et sa réactivité.
Des exemples d’éléments à haute électronégativité comprennent le fluor, l’oxygène et l’azote.
