Le fumarate de diméthyle (DMF) est un composé utilisé en médecine pour traiter la sclérose en plaques. Il réduit les taux d’inflammation et de rechute en modulant le système immunitaire.
| Nom de l’UICPA | Ester diméthylique de l’acide (E)-but-2-ènedioïque |
| Formule moléculaire | C6H8O4 |
| Numero CAS | 624-49-7 |
| Synonymes | DMF, Bioban, Fumaderm, Tecfidera, Diméthyl (E)-butènedioate |
| InChI | InChI=1S/C6H8O4/c1-9-5(7)3-4-6(8)10-2/h3-4H,1-2H3/b4-3+ |
Propriétés du fumarate de diméthyle
Formule de fumarate de diméthyle
La formule chimique du fumarate de diméthyle est C6H8O4. Il représente la disposition spécifique et les types d’atomes présents dans le composé, composé de 6 atomes de carbone (C), 8 atomes d’hydrogène (H) et 4 atomes d’oxygène (O). La formule fournit une représentation concise de la composition élémentaire du fumarate de diméthyle.
Fumarate De Diméthyle Masse molaire
La masse molaire du DMF est calculée en additionnant les masses atomiques de tous ses éléments constitutifs. Avec une formule moléculaire de C6H8O4, la masse molaire est d’environ 144,13 grammes par mole. Cette valeur est cruciale pour divers calculs et conversions chimiques impliquant le DMF.
Point d’ébullition du fumarate de diméthyle
Le DMF présente un point d’ébullition d’environ 191 degrés Celsius (376 degrés Fahrenheit). Le point d’ébullition signifie la température à laquelle le composé liquide passe à l’état gazeux, et dans le cas du DMF, cela se produit à cette température particulière.
Fumarate de diméthyle Point de fusion
Le point de fusion du DMF est d’environ 102 degrés Celsius (216 degrés Fahrenheit). Cette température représente le point auquel la forme solide du composé passe à l’état liquide. Le DMF subit ce changement de phase au point de fusion spécifié.
Densité du fumarate de diméthyle g/mL
Le DMF possède une densité d’environ 1,30 grammes par millilitre (g/mL). La densité est une mesure de la masse contenue dans un volume spécifique d’une substance. Dans le cas du DMF, il indique la concentration massique dans chaque millilitre du composé.
Fumarate De Diméthyle Poids moléculaire
Le poids moléculaire du DMF, également appelé masse molaire, est d’environ 144,13 grammes par mole. C’est la somme des poids atomiques de tous les atomes présents dans une molécule de DMF. Le poids moléculaire est crucial pour divers calculs et analyses chimiques.
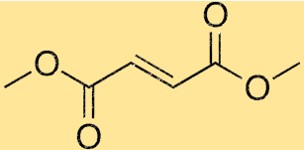
Structure du fumarate de diméthyle
La structure du DMF se compose de deux groupes méthyle (CH3) attachés à un fragment fumarate central. Le fragment fumarate est constitué de deux groupes carboxylate reliés par une double liaison. Cette disposition confère au DMF sa forme caractéristique et ses propriétés chimiques.
Solubilité du fumarate de diméthyle
Le DMF est peu soluble dans l’eau mais se dissout facilement dans les solvants organiques comme l’éthanol ou le méthanol. Cette solubilité limitée dans l’eau est un facteur à prendre en compte lorsque l’on travaille avec le DMF et ses applications dans diverses industries.
| Apparence | Cristaux incolores ou poudre blanche |
| Gravité spécifique | 1h30 |
| Couleur | Incolore |
| Odeur | Inodore |
| Masse molaire | 144,13 g/mole |
| Densité | 1,30 g/ml |
| Point de fusion | 102 °C (216 °F) |
| Point d’ébullition | 191 °C (376 °F) |
| Point d’éclair | Pas disponible |
| Solubilité dans l’eau | Peu soluble |
| Solubilité | Soluble dans les solvants organiques (par exemple, éthanol, méthanol) |
| Pression de vapeur | Pas disponible |
| Densité de vapeur | Pas disponible |
| pKa | Pas disponible |
| pH | Pas disponible |
Sécurité et dangers du fumarate de diméthyle
Le DMF doit être manipulé avec soin pour garantir la sécurité. Il peut provoquer une irritation en cas de contact avec la peau, les yeux ou le système respiratoire. Une ventilation adéquate et des équipements de protection, tels que des gants et des lunettes, sont recommandés lors de son utilisation. L’ingestion ou l’inhalation de DMF doit être évitée, car cela peut entraîner des risques pour la santé. En cas d’exposition accidentelle, des soins médicaux immédiats sont nécessaires. Il est important de suivre les directives de stockage appropriées et de garder le composé à l’écart des flammes nues ou des sources de chaleur. Le respect des protocoles de sécurité minimise les risques associés au DMF.
| Symboles de danger | Aucun |
| Description de la sécurité | Évitez tout contact avec la peau, les yeux et le système respiratoire. Assurer une ventilation adéquate. Portez des équipements de protection (gants, lunettes). Évitez l’ingestion et l’inhalation. Consulter immédiatement un médecin en cas d’exposition. Conserver à l’écart des flammes nues ou des sources de chaleur. |
| Numéros d’identification de l’ONU | N’est pas applicable |
| Code SH | 2917.19.90 |
| Classe de danger | Non classés |
| Groupe d’emballage | N’est pas applicable |
| Toxicité | Peut provoquer une irritation de la peau et des yeux. Évitez l’ingestion et l’inhalation. |
Méthodes de synthèse du fumarate de diméthyle
Il existe différentes méthodes de synthèse du DMF.
Une approche courante implique l’estérification de l’acide fumarique à l’aide de méthanol . Dans cette réaction, l’acide sulfurique ou l’acide p-toluènesulfonique sert de catalyseur acide pour combiner l’acide fumarique avec le méthanol . La réaction se déroule dans des conditions de reflux, généralement à une température élevée, pour faciliter le processus d’estérification. Le catalyseur acide favorise activement la réaction en facilitant l’élimination de l’eau, qu’il provoque comme sous-produit.
Une autre méthode implique la réaction de l’anhydride maléique avec le méthanol . L’anhydride maléique et le méthanol réagissent en présence d’un catalyseur acide, tel que l’acide sulfurique ou l’acide phosphorique, pour donner du DMF. La réaction se produit par l’ouverture du cycle anhydride cyclique et l’estérification ultérieure.
Pour préparer le DMF, on peut effectuer une réaction de transestérification en utilisant du maléate de diméthyle. Dans ce processus, le maléate de diméthyle réagit avec le méthanol alors qu’un catalyseur, tel que le méthylate de sodium ou l’hydroxyde de potassium , est présent. La réaction de transestérification conduit à la formation de DMF.
Ces méthodes de synthèse fournissent des voies pour obtenir du DMF en laboratoire ou en milieu industriel. Des facteurs tels que l’efficacité, le rendement et la disponibilité des matières premières déterminent le choix de chaque méthode, car chaque méthode présente ses propres avantages. Un contrôle approprié des conditions de réaction et des étapes de purification est important pour garantir la pureté et la qualité souhaitées du DMF synthétisé.
Utilisations du fumarate de diméthyle
Le DMF trouve des applications dans divers domaines en raison de ses diverses propriétés. Voici quelques utilisations du DMF :
- Traitement de la sclérose en plaques : La FDA a approuvé le DMF comme médicament pour traiter les formes récurrentes de sclérose en plaques. Il aide à réduire les taux de rechute et l’inflammation en modulant le système immunitaire.
- Industrie pharmaceutique : les composés pharmaceutiques utilisent le DMF comme intermédiaire dans leur synthèse. Il sert de base à la production de divers médicaments.
- Agent antimicrobien : Le DMF démontre des propriétés antimicrobiennes. Il trouve une application comme conservateur dans des produits tels que les peintures, les revêtements et les adhésifs. Il aide à inhiber la croissance des micro-organismes et à prévenir la détérioration.
- Industrie textile : L’industrie textile utilise le DMF comme biocide puissant pour inhiber la croissance de moisissures et de champignons sur les tissus pendant le stockage et le transport.
- Meubles et articles en cuir : Dans la production de meubles, d’articles en cuir et de chaussures, les fabricants utilisent le DMF comme inhibiteur de moisissure. Il aide à protéger ces articles contre les dommages microbiens pendant le stockage et le transport.
- Stabilisateur de polymère : Le DMF agit comme stabilisant et antioxydant dans les polymères, tels que le polypropylène et le polyéthylène. Cela contribue à améliorer leur stabilité thermique et à prolonger leur durée de conservation.
- Réactif chimique : Diverses réactions chimiques, notamment les estérifications et les transestérifications, utilisent le DMF comme réactif. Il facilite la synthèse des esters et autres composés organiques.
Ce ne sont là que quelques exemples des diverses applications du DMF dans tous les secteurs. Ses propriétés uniques en font un composé précieux dans les domaines de la médecine, de la fabrication, de la conservation et de la chimie.
Des questions:
Q : Comment éliminer le fumarate de diméthyle des meubles ?
R : Le DMF peut être retiré des meubles en essuyant les zones affectées avec une solution savonneuse douce ou en utilisant un agent de nettoyage spécialement conçu pour éliminer les taches et les résidus.
Q : Qu’est-ce qui est le plus polaire, le maléate de diéthyle ou le fumarate de diméthyle ?
R : Le DMF est plus polaire que le maléate de diéthyle en raison de la présence de groupes carbonyle attracteurs d’électrons dans sa structure.
Q : À quoi sert le fumarate de diméthyle ?
R : Le DMF est utilisé dans le traitement de la sclérose en plaques et trouve également des applications dans l’industrie pharmaceutique, comme conservateur, ainsi que dans les industries du textile et des polymères.
Q : Quels sont les deux groupes fonctionnels présents dans le maléate de diméthyle et le fumarate de diméthyle ?
R : Le maléate de diméthyle et le DMF contiennent tous deux des groupes fonctionnels ester et alcène.
Q : Peut-on être allergique à l’odeur du fumarate de diméthyle ?
R : Oui, certaines personnes peuvent développer des réactions allergiques à l’odeur du DMF, entraînant des symptômes tels qu’une irritation cutanée, des problèmes respiratoires ou une dermatite allergique.
Q : Le maléate de diméthyle et le fumarate de diméthyle sont-ils réversibles ?
R : Non, le maléate de diméthyle et le DMF ne sont pas réversibles. Ce sont des isomères différents du même composé et ne s’interconvertissent pas facilement.
Q : Quelle technique de laboratoire utiliserez-vous pour purifier le produit de réaction, le fumarate de diméthyle ?
R : La distillation est couramment utilisée pour purifier le produit de réaction DMF en le séparant des impuretés en fonction des différences de points d’ébullition.
