Le 2-pentanol est un composé organique de formule moléculaire C5H12O. C’est un liquide incolore utilisé comme solvant et dans la production de produits pharmaceutiques et de parfums.
| Nom UICPA | 2-pentanol |
| Formule moléculaire | C5H12O |
| Numero CAS | 6032-29-7 |
| Synonymes | Alcool amylique, alcool sec-amylique, alcool 2-pentylique |
| InChI | InChI=1S/C5H12O/c1-3-4-5(2)6/h5-6H,3-4H2,1-2H3 |
Propriétés du 2-pentanol
Formule 2-pentanol
La formule du 2-pentanol est C5H12O. Il représente la composition moléculaire de ce composé organique. Il se compose de cinq atomes de carbone, douze atomes d’hydrogène et un atome d’oxygène.
2-Pentanol Masse molaire
La masse molaire de l’alcool 2-pentylique est calculée en additionnant les masses atomiques de ses éléments constitutifs. Avec une formule de C5H12O, sa masse molaire est d’environ 88,15 grammes par mole. La masse molaire est cruciale pour divers calculs et conversions chimiques.
Point d’ébullition du 2-pentanol
Le point d’ébullition de l’alcool 2-pentylique est la température à laquelle il passe d’un liquide à un gaz sous pression atmosphérique standard. Son point d’ébullition est relativement bas, environ 118 degrés Celsius (244 degrés Fahrenheit). Cette propriété le rend utile dans divers processus industriels.
2-Pentanol Point de fusion
Le point de fusion de l’alcool 2-pentylique fait référence à la température à laquelle il passe de l’état solide à l’état liquide. Son point de fusion est d’environ -79 degrés Celsius (-110 degrés Fahrenheit). Cette caractéristique lui permet d’exister sous forme liquide à température ambiante.
Densité du 2-pentanol g/mL
La densité de l’alcool 2-pentylique est une mesure de sa masse par unité de volume. Sa densité est d’environ 0,81 gramme par millilitre (g/mL). Cette propriété est importante pour déterminer la solubilité et le comportement physique du composé.
2-Pentanol Poids moléculaire
Le poids moléculaire de l’alcool 2-pentylique est la somme des poids atomiques de tous les atomes de sa formule. C’est environ 88,15 grammes par mole. Le poids moléculaire donne un aperçu de la masse du composé et aide à divers calculs chimiques.
Structure du 2-pentanol
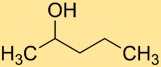
La structure de l’alcool 2-pentylique est constituée d’une chaîne de cinq atomes de carbone liés les uns aux autres, avec un groupe hydroxyle (-OH) attaché au deuxième carbone. Cette structure d’alcool primaire confère au composé des propriétés chimiques et une réactivité uniques.
Solubilité du 2-pentanol
L’alcool 2-pentylique présente une solubilité modérée dans l’eau, en raison de sa capacité à former des liaisons hydrogène. Il est plus soluble dans les solvants polaires comme l’éthanol et l’acétone. Cependant, sa solubilité diminue avec l’augmentation de la longueur de la chaîne carbonée dans les solvants non polaires.
| Apparence | Liquide incolore |
| Gravité spécifique | 0,812 g/ml |
| Couleur | Incolore |
| Odeur | Odeur caractéristique |
| Masse molaire | 88,15 g/mole |
| Densité | 0,812 g/ml |
| Point de fusion | -79 °C |
| Point d’ébullition | 118 °C |
| Point d’éclair | 34 °C |
| Solubilité dans l’eau | Miscible |
| Solubilité | Soluble dans les solvants polaires tels que l’éthanol et l’acétone |
| La pression de vapeur | 5,15 mmHg à 25 °C |
| Densité de vapeur | 3,03 (air = 1) |
| pKa | 16,0 |
| pH | Environ 7 |
Sécurité et dangers du 2-pentanol
L’alcool 2-pentylique soulève certaines considérations de sécurité et de danger. Il est important de manipuler ce composé avec précaution. L’inhalation de ses vapeurs peut provoquer une irritation du système respiratoire. Le contact direct avec la peau ou les yeux peut entraîner une irritation et un inconfort. Il est conseillé d’utiliser un équipement de protection approprié, tel que des gants et des lunettes, lorsque vous travaillez avec de l’alcool 2-pentylique. Ce composé est inflammable et doit être tenu à l’écart des flammes nues ou des sources d’inflammation. En cas d’ingestion ou d’exposition accidentelle, il est recommandé de consulter un médecin. Il est essentiel de stocker et de manipuler l’alcool 2-pentylique dans un endroit bien ventilé et de suivre les protocoles de sécurité appropriés.
| Symboles de danger | Xn (nocif) |
| Description de la sécurité | Évitez l’inhalation, portez un équipement de protection |
| Numéros d’identification de l’ONU | ONU 1105 |
| Code SH | 2905.16.00 |
| Classe de danger | 3 |
| Groupe d’emballage | III |
| Toxicité | Nocif en cas d’ingestion ou d’inhalation |
Méthodes de synthèse du 2-pentanol
Il existe plusieurs méthodes de synthèse de l’alcool 2-pentylique. Une approche courante est la réaction d’hydroboration-oxydation. Dans cette méthode, le 1-pentène, un alcène, subit une hydroboration avec du borane pour former l’alcoxyde de bore correspondant. Une oxydation ultérieure à l’aide de peroxyde d’hydrogène ou d’hypochlorite de sodium convertit l’alcoolate de bore en alcool 2-pentylique.
Une autre méthode implique l’hydratation du 1-pentène. Dans ce processus, le 1-pentène réagit avec l’eau en présence d’un catalyseur acide tel que l’acide sulfurique ou l’acide phosphorique. La réaction se déroule par addition de Markovnikov, entraînant la formation d’alcool 2-pentylique.
Pour synthétiser l’alcool 2-pentylique, on peut réduire le pentanal, un aldéhyde, en utilisant des agents réducteurs tels que le borohydrure de sodium ou l’hydrure de lithium et d’aluminium. La réaction convertit le pentanal en alcool 2-pentylique.
La réaction de Grignard permet la préparation de l’alcool 2-pentylique. La réaction d’un réactif de Grignard, tel que le bromure de méthylmagnésium, avec du formaldéhyde (ou ses dérivés) génère un intermédiaire alcoxyde de magnésium. Le traitement acide de l’intermédiaire donne de l’alcool 2-pentylique.
La fermentation est une autre méthode pour obtenir de l’alcool 2-pentylique. Certains micro-organismes, comme la levure, peuvent convertir les sucres issus de la biomasse en alcool 2-pentylique grâce à une série de réactions enzymatiques.
Ces méthodes de synthèse offrent diverses voies pour produire de l’alcool 2-pentylique, offrant une flexibilité pour les applications industrielles et garantissant un approvisionnement constant de ce composé précieux.
Utilisations du 2-pentanol
L’alcool 2-pentylique a de nombreuses applications en tant que solvant dans diverses industries, notamment les produits pharmaceutiques, les cosmétiques et les parfums.
- Il est utilisé comme intermédiaire chimique dans la production de plastifiants, d’arômes et de composés pharmaceutiques.
- L’alcool 2-pentylique est utilisé comme matière première pour la synthèse d’autres composés, tels que les esters, en le faisant réagir avec des acides.
- Il est utilisé comme modificateur de viscosité dans les produits de soins personnels et comme agent mouillant dans les revêtements et les peintures.
- L’alcool 2-pentylique est utilisé comme solvant pour les résines, les huiles et les cires en raison de sa capacité à dissoudre un large éventail de substances.
- Il sert de matière première pour la fabrication de détergents, d’émulsifiants et de tensioactifs.
- Ce composé est utilisé comme agent aromatisant dans les aliments et les boissons, ajoutant des notes fruitées et florales au produit final.
- L’alcool 2-pentylique est utilisé dans la production de produits chimiques agricoles, tels que des herbicides et des insecticides.
- Il agit comme un réactif chimique en synthèse organique, facilitant diverses transformations chimiques.
- L’alcool 2-pentylique est également utilisé en laboratoire comme solvant pour les processus d’extraction et de purification.
Des questions:
Q : Quelle est la fonction du catalyseur acide pour favoriser la déshydratation du 2-pentanol ?
R : Le catalyseur acide facilite l’élimination d’une molécule d’eau de l’alcool 2-pentylique, favorisant la réaction de déshydratation et la formation de l’alcène correspondant.
Q : Comment fabriquer du 2-pentanol avec une réaction de Grignard ?
R : Pour synthétiser l’alcool 2-pentylique à l’aide d’une réaction de Grignard, faites réagir un réactif de Grignard, tel que le bromure de méthylmagnésium, avec du formaldéhyde ou ses dérivés, suivi d’un traitement acide pour produire de l’alcool 2-pentylique.
Q : Quel est le spectre de masse du 2-pentanol ?
R : Le spectre de masse de l’alcool 2-pentylique affiche la distribution de ses ions et fragments moléculaires, fournissant des informations sur son poids moléculaire et ses caractéristiques structurelles.
